X-ray_crystallography
X線結晶学(XRC)の原子及び分子構造を決定する実験科学である結晶の結晶構造は、入射ビーム引き起こした、X線をする回折多くの特定の方向にこれらの回折ビームの角度と強度を測定することにより、結晶学者は結晶内の電子密度の3次元画像を作成できます。この電子密度から、結晶内の原子の平均位置、化学結合、結晶学的無秩序、およびその他のさまざまな情報を決定できます。
粉末X線回折装置の動きに
塩、金属、鉱物、半導体、さまざまな無機、有機、生体分子など、多くの材料が結晶を形成する可能性があるため、X線結晶構造解析は多くの科学分野の発展の基礎となっています。この方法は、最初の数十年間の使用で、原子のサイズ、化学結合の長さと種類、およびさまざまな材料、特に鉱物と合金の間の原子スケールの違いを決定しました。この方法はまた、ビタミン、薬物、タンパク質、DNAなどの核酸を含む多くの生体分子の構造と機能を明らかにしました。X線結晶学は、新しい材料の原子構造を特徴づけるための、そして他の実験によって類似しているように見える識別可能な材料において、依然として主要な方法です。X線結晶構造は、材料の異常な電子的または弾性的特性を説明したり、化学的相互作用やプロセスに光を当てたり、病気に対する医薬品を設計するための基礎として機能したりすることもできます。
単結晶X線回折測定では、結晶がゴニオメーターに取り付けられます。ゴニオメーターは、結晶を選択した方向に配置するために使用されます。結晶は、細かく集束された単色のX線ビームで照らされ、反射と呼ばれる規則的な間隔のスポットの回折パターンを生成します。異なる方向で撮影された2次元画像は、サンプルで知られている化学データと組み合わせて、フーリエ変換の数学的方法を使用して、結晶内の電子密度の3次元モデルに変換されます。結晶が小さすぎる場合、または内部構成が十分に均一でない場合は、解像度が低い(あいまいさ)、またはエラーが発生する可能性が
X線結晶学は、原子構造を決定するための他のいくつかの方法に関連しています。同様の回折パターンは、電子または中性子を散乱させることによって生成できます。これらは、フーリエ変換によって同様に解釈されます。十分なサイズの単結晶が得られない場合は、他のさまざまなX線法を適用して、より詳細でない情報を取得できます。このような方法には、繊維回折、粉末回折、および(サンプルが結晶化されていない場合)小角X線散乱(SAXS)が含まれます。調査中の材料がナノ結晶粉末の形でしか入手できない場合、または結晶化度が低い場合は、電子結晶学の方法を適用して原子構造を決定できます。
上記のすべてのX線回折法では、散乱は弾性的です。散乱X線は入射X線と同じ波長を持っています。対照的に、非弾性X線散乱法は、原子の分布ではなく、プラズモン、結晶場および軌道励起、マグノン、フォノンなどのサンプルの励起を研究するのに役立ちます。
コンテンツ
1 歴史
1.1 結晶とX線の初期の科学史 1.2 X線回折 1.3 散乱 1.4 1912年から1920年までの開発 1.5 文化的および美的重要性
2 化学および材料科学への貢献
2.1 鉱物学および冶金学 2.2 初期の有機および小さな生体分子 2.3 生体高分子結晶学
3 散乱技術
3.1 弾性散乱と非弾性散乱 3.2 その他のX線技術 3.3 電子および中性子回折
4 メソッド
4.1 単結晶X線回折の概要
4.1.1 手順
4.1.2 制限事項
4.2 結晶 4.3 データ収集
4.3.1 クリスタルの取り付け
4.3.2 X線源
4.3.2.1 回転陽極
4.3.2.2 マイクロフォーカスチューブ
4.3.2.3 放射光
4.3.2.4 自由電子レーザー
4.3.3 反射を記録する
4.4 データ分析
4.4.1 結晶対称性、ユニットセル、および画像スケーリング
4.4.2 初期フェーズ
4.4.3 モデル構築とフェーズの改良
4.4.4 障害
4.4.5 応用計算データ分析
4.5 構造物の堆積
5 回折理論
5.1 ブラッグの法則による直感的な理解 5.2 フーリエ変換としての散乱 5.3 フリーデルとビボエの仲間 5.4 エワルド球 5.5 パターソン関数 5.6 クリスタルの利点
6 X線結晶学を含むノーベル賞
7 アプリケーション
7.1 薬物の識別 7.2 ナノマテリアル、繊維、ポリマーの特性評価 7.3 骨の調査 7.4 集積回路
8 も参照してください
9 参考文献
10 参考文献
10.1 結晶学のための国際的な表 10.2 記事のバインドされたコレクション 10.3 教科書 10.4 応用計算データ分析 10.5 歴史的
11 外部リンク
11.1 チュートリアル 11.2 一次データベース 11.3 派生データベース 11.4 構造検証
歴史
結晶とX線の初期の科学史

ケプラーの法則、 Strena seu de Nive Sexangulaからの正方形(図A、上)と六角形(図B、下)のパッキングの図 結晶は、その規則性と対称性で長い間賞賛されていましたが、17世紀まで科学的に調査されていませんでした。Johannes Keplerは、彼の作品Strena seu de Nive Sexangula(Hexagonal Snowの新年の贈り物)(1611)で、スノーフレーク結晶の六角形の対称性は球形の水粒子の規則的なパッキングによるものであると仮定しました。

X線結晶学で示されているように、雪片の六角形の対称性は、各水分子の周りの水素結合の四面体配列に
起因し
ます。水分子は、と同様に配置された
シリコンの原子
トリジマイト多形のSiO
2。得られた結晶構造は、主軸に沿って見たときに六角形の対称性を持っています。
デンマークの科学者ニコラス・ステノ(1669)は、結晶対称性の実験的調査の先駆者です。ステノは面間の角度は、結晶の特定のタイプのすべての標本において同じであることを示したとルネ=ジュスト・アユイ結晶のすべての面が同一のブロックの単純な積層パターンによって記述することができることを発見した(1784)形とサイズ。したがって、1839年にウィリアムハロウズミラーは、各面に3つの小さな整数の一意のラベルを付けることができました。ミラー指数は、結晶面を識別するために現在も使用されています。Haüyの研究は、結晶が原子と分子の規則的な3次元配列(Bravais格子)であるという正しい考えにつながりました。単一のユニットセルは、必ずしも垂直である必要はない3つの主要な方向に沿って無期限に繰り返されます。19世紀では、結晶の可能な対称性の完全なカタログはによって働いたヨハンヘッセル、アウグストブラベ、エブグラフ・フェドロブ、アーサーSchönflies (遅れて)、およびウィリアム・バーロウ(1894 )。入手可能なデータと物理的推論から、Barlowは1880年代にいくつかの結晶構造を提案し、後でX線結晶学によって検証されました。しかしながら、1880年代には入手可能なデータが少なすぎて、彼のモデルを決定的なものとして受け入れることができませんでした。
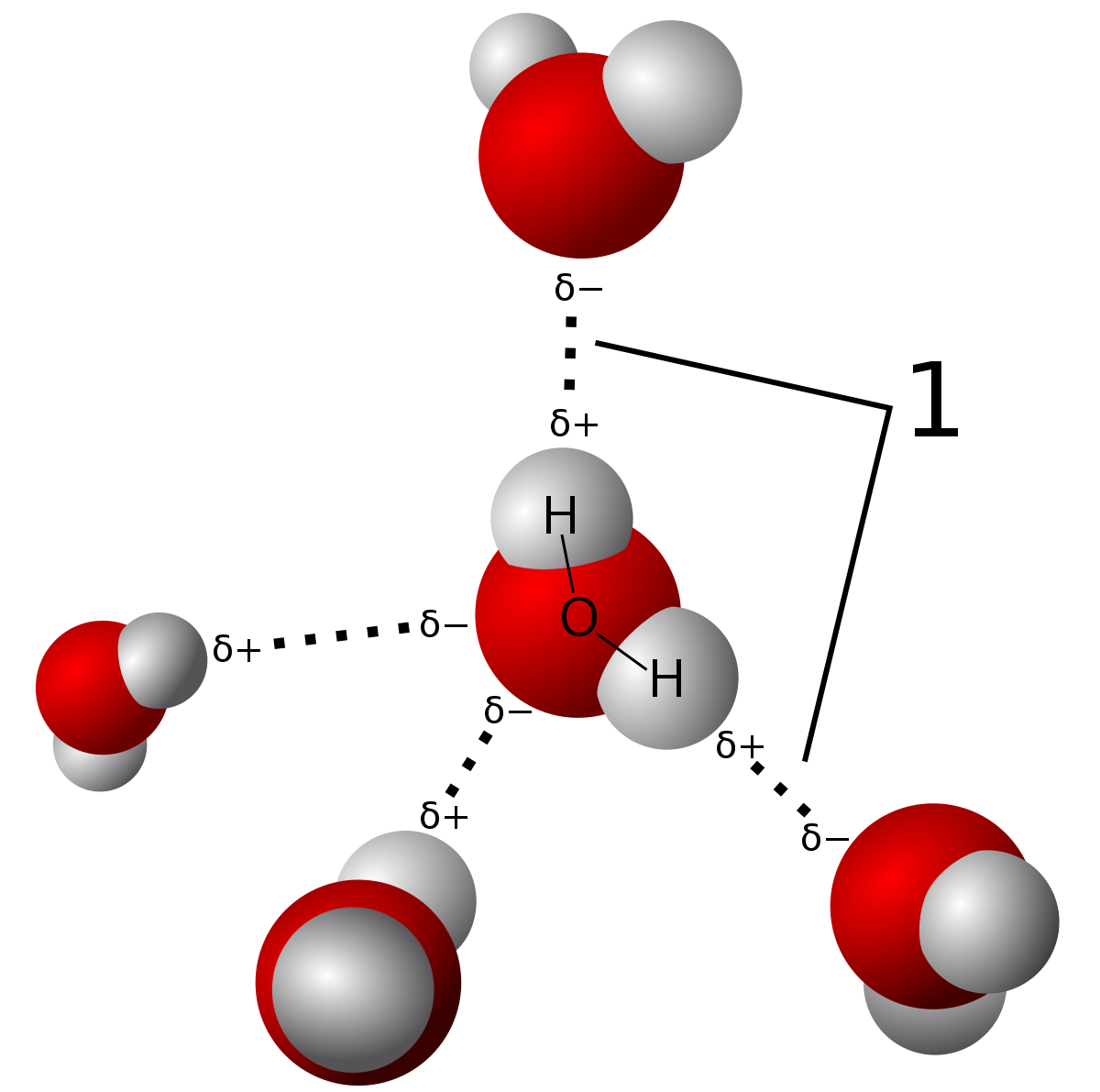
X線結晶学は、氷中の水分子の配置を示し、固体を一緒に保持している水素結合(1)を明らかに
します。このような精度(解像度)で物質の構造を決定できる方法は他にほとんどありません ヴィルヘルム・レントゲンは、結晶対称性の研究が完了したちょうどその時、1895年にX線を発見しました。物理学者はX線の性質について確信が持てませんでしたが、すぐにそれらが光の一種である電磁放射の波であると疑われました。電磁放射のマクスウェル理論は科学者の間で広く受け入れられており、チャールズ・グローバー・バークラによる実験では、X線が可視波長で観察されるものと同様の横偏波やスペクトル線などの電磁波に関連する現象を示すことが示されました。アーノルドゾンマーフェルトの実験室でのシングルスリット実験は、X線が約1オングストロームの波長を持っていることを示唆しました。X線は波であるだけでなく光子でもあり、粒子の性質を持っています。アルバート・アインシュタインは、1905年に光子の概念を導入したが、それは、広く1922まで受け入れられなかった アーサーコンプトン電子からのX線の散乱によってそれを確認しました。ガスのイオン化など、X線の粒子のような特性により、1907年にウィリアムヘンリーブラッグはX線は電磁放射ではないと主張しました。 ブラッグの見解は人気がなく、1912年のマックスフォンラウエによるX線回折の観察は、ほとんどの科学者にとってX線が電磁放射の一種であることを確認した。
X線回折

入ってくるビーム(左上から来る)により、各散乱体はその強度のごく一部を球面波として再放射します。散乱体が分離して対称に配置されている場合
、Dは、これらの球面波は、それらの経路長差2方向に(建設追加)同期であろう
次元の整数倍に等しいθ罪
波長λを。その場合、入射ビームの一部が角度2θだけ偏向され、回折パターンに反射スポットが
生成され 結晶は原子の規則的な配列であり、X線は電磁放射の波と見なすことができます。原子は、主に原子の電子を介してX線波を散乱させます。灯台に当たる海の波が灯台から発する二次球面波を生成するのと同じように、電子に当たるX線は電子から発する二次球面波を生成します。この現象は弾性散乱として知られており、電子(または灯台)は散乱体として知られています。散乱体の規則的な配列は、球面波の規則的な配列を生成します。これらの波は、破壊的な干渉によってほとんどの方向で互いに打ち消し合いますが、ブラッグの法則によって決定されるいくつかの特定の方向に建設的に追加されます。 λ= 2sin θ
{n lambda = 2d sin theta}
ここで、dは回折面間の間隔です。 θ { theta}
は入射角、nは任意の整数、λはビームの波長です。これらの特定の方向は、反射と呼ばれる回折パターン上のスポットとして表示されます。したがって、X線回折は、電磁波(X線)が散乱体の規則的な配列(結晶内の原子の繰り返し配置)に衝突することから生じます。
X線は、波長λが通常、結晶内の平面間の間隔dと同じ桁(1〜100オングストローム)であるため、回折パターンを生成するために使用されます。原則として、1665年にフランチェスコマリアグリマルディによって最初に予測されたように、散乱体の規則的な配列に衝突する波は回折を生成します。有意な回折を生成するには、散乱体間の間隔と衝突波の波長のサイズが同じである必要が説明のために、鳥の羽を通る太陽光の回折は、17世紀後半にジェームズグレゴリーによって最初に報告されました。可視光用の最初の人工回折格子は、1787年にDavid Rittenhouseによって、1821年にJoseph von Fraunhoferによって構築されました。ただし、可視光の波長は長すぎて(通常、5500オングストローム)、結晶からの回折を観察できません。最初のX線回折実験の前は、結晶内の格子面間の間隔は確実にわかっていませんでした。
結晶として使用することができるとの考え回折格子のためのX線は、間の会話の中で1912年に生まれたポール・ピーター・エワルドとマックス・フォン・ラウエでイングリッシュガーデンでミュンヘン。Ewaldは彼の論文のために結晶の共振器モデルを提案しましたが、波長が共振器間の間隔よりもはるかに大きいため、このモデルは可視光を使用して検証できませんでした。フォンラウエは、このような小さな間隔を観察するには、より短い波長の電磁放射が必要であることに気づき、X線が結晶のユニットセル間隔に匹敵する波長を持っている可能性があることを示唆しました。フォンラウエは、2人の技術者、ウォルターフリードリッヒと彼のアシスタントであるポールクニッピングと協力して、硫酸銅結晶を通してX線のビームを照射し、その回折を写真乾板に記録しました。開発後、プレートは、中央のビームによって生成されたスポットの周りに交差する円のパターンで配置された多数の明確なスポットを示しました。 フォン・ラウエは、結晶内の散乱角とユニットセル間隔のサイズと方向を結び付ける法則を開発し、1914年にノーベル物理学賞を受賞しました。
散乱
以下の数学的導出で説明されているように、X線散乱は結晶内の電子密度によって決定されます。X線のエネルギーは価電子のエネルギーよりもはるかに大きいため、散乱は、電磁光線と自由電子との相互作用であるトムソン散乱としてモデル化できます。このモデルは、一般に、散乱放射線の偏光を記述するために採用されます。
質量mおよび電気素量qの1つの粒子のトムソン散乱の強度は次のとおりです。I o = I e(( 4 2 4 )。 1 + cos2 2 θ 2 = I e
7.94.10
−26 1+ cos2 2 θ 2 = I
e {I_ {o} = I_ {e} left({ frac {q ^ {4}} {m ^ {2} c ^ {4}}} right){ frac {1+ cos ^ {2} 2 theta} {2}} = I_ {e} 7.94.10 ^ {-26} { frac {1+ cos ^ {2} 2 theta} {2}} = I_ {e} f }
したがって、電子よりもはるかに重い原子核は、散乱X線にほとんど寄与しません。
1912年から1920年までの開発

が ダイヤモンド(上部左)と
グラファイト(右上)は、化学的に同一であり、両方の純粋な組成である
炭素-X線結晶学は、(下)は、それらの原子の配列を明らかにし、それらの異なる特性を占めます。ダイヤモンドでは、炭素原子が四面体に配置さ
れ、単一の共有結合によって結合され
ているため、すべての方向に強くなります。対照的に、グラファイトは積み重ねられたシートで構成されています。シート内では、結合は共有結合であり、六角形の対称性がありますが、シート間に共有結合がないため、グラファイトが簡単にフレークに切断されます。
フォンラウエの先駆的な研究の後、この分野は急速に発展しました。特に、物理学者のウィリアムローレンスブラッグと彼の父親のウィリアムヘンリーブラッグによって開発されました。1912年から1913年に、若いブラッグはブラッグの法則を開発しました。これは、観測された散乱を結晶内の等間隔の平面からの反射と結び付けます。 父と息子のブラッグスは、結晶学での業績に対して1915年のノーベル物理学賞を共有した。初期の構造は一般的に単純で、1次元の対称性が特徴でした。しかし、計算および実験方法が次の数十年で改善されるにつれて、ユニットセル内の原子のより複雑な2次元および3次元配置の信頼できる原子位置を推定することが可能になりました。
分子や鉱物の構造を決定するためのX線結晶学の可能性は、化学実験や流体力学的実験からは漠然としか知られていませんでしたが、すぐに実現しました。初期の構造は単純な無機結晶と鉱物でしたが、これらでさえ物理学と化学の基本法則を明らかにしました。1914年に「解決」された(つまり決定された)最初の原子分解能構造は、テーブルソルトの構造でした。 食卓塩構造における電子の分布は、結晶が必ずしも共有結合した分子で構成されているとは限らないことを示し、イオン性化合物の存在を証明しました。ダイヤモンドの構造は同じ年に解決され、 化学結合の四面体配列が証明され、C–C単結合の長さが1.52オングストロームであることが示されました。他の初期の構造には、銅、 フッ化カルシウム(CaF 2、蛍石としても知られている)、方解石(CaCO 3)、黄鉄鉱(FeS 2)が含まれていました。1915年のスピネル(MgAl 2 O 4)。 1916年の二酸化チタン(TiO 2)のルチル型およびアナターゼ型。 1919年にパイロクロイトMn(OH)2、ひいてはブルーサイトMg(OH)2。 1919年にも、硝酸ナトリウム(NaNO 3)と二ヨウ化セシウム(CsICl 2)がラルフによって測定されました。Walter Graystone Wyckoff、およびウルツ鉱(六方晶ZnS)構造は1920年に知られるようになりました。
構造グラファイトは1916年に解決されたの関連する方法により粉末回折、によって開発されたピーター・デバイとポールシェラーにより、独立して、およびアルバートハル1917年黒鉛の構造を決定しました。独立して2つのグループによる1924年の単結晶回折から。 ハルはまた、粉末法を使用して、鉄やマグネシウムなどのさまざまな金属の構造を決定しました。
文化的および美的重要性
1951年に、で祭りのパターン・グループ、英国の祭りは、のX線結晶構造解析に基づく設計レースやプリントにテキスタイルメーカーと経験豊富な結晶学者の共同のグループを主催し、インスリン、陶土、およびヘモグロビン。このプロジェクトの主要な科学者の1人は、当時ケンブリッジのキャベンディッシュ研究所の研究助手であったヘレン・メーガウ博士(1907–2002)でした。Megawは、結晶図からインスピレーションを得て、デザインの可能性を見出した中心人物の1人として認められています。 2008年、ロンドンのウェルカムコレクションは、「アトムからパターンへ」と呼ばれるフェスティバルパターングループの展示会をキュレーションしました。
化学および材料科学への貢献
X線結晶学は、化学結合と非共有相互作用のより良い理解につながりました。初期の研究では、原子の典型的な半径が明らかになり、ダイヤモンド構造の炭素の四面体結合、ヘキサクロロ白金酸アンモニウム(IV)で観察された金属の八面体結合など、化学結合の多くの理論モデルが確認されました。平面炭酸基および芳香族分子で観察された共鳴。 キャスリーンロンズデールの1928年のヘキサメチルベンゼンの構造は、ベンゼンの六角形の対称性を確立し、脂肪族C-C結合と芳香族C-C結合の結合長に明らかな違いを示しました。この発見は、化学結合間の共鳴のアイデアにつながり、それは化学の発展に深刻な結果をもたらしました。彼女の結論は、分子置換の初期の形態である他の分子に基づいて、1921年にナフタレンとアントラセンのモデルを発表したウィリアム・ヘンリー・ブラッグによって予想された。
また、1920年代に、ヴィクトール・モーリッツ・ゴールドシュミットとその後のライナス・ポーリングは、化学的にありそうもない構造を排除し、原子の相対的なサイズを決定するための規則を開発しました。これらの規則は、ブルッカイト(1928)の構造と、二酸化チタンのルチル、ブルッカイト、アナターゼ型の相対的な安定性の理解につながりました。
2つの結合原子間の距離は、結合強度とその結合次数の敏感な尺度です。したがって、X線結晶構造解析により、金属-金属二重結合 金属-金属四重結合 など、無機化学におけるさらにエキゾチックなタイプの結合が発見されました。 55] および3中心、2電子結合。 X線結晶学、または厳密に言えば、非弾性コンプトン散乱実験は、水素結合の部分的な共有結合特性の証拠も提供しています。の分野では、有機金属化学、のX線構造フェロセンの科学的研究を開始したサンドイッチ化合物、 のものとしながら、ツァイゼ塩「バック・ボンディング」と金属-π錯体の研究を刺激しました。 最後に、X線結晶学は、超分子化学の開発、特にクラウンエーテルの構造とホスト-ゲスト化学の原理の解明において先駆的な役割を果たしました。
X線回折は、触媒開発において非常に強力なツールです。材料の結晶構造をチェックしたり、新しい構造を解明したりするために、Ex-situ測定が定期的に実行されます。その場実験は、反応条件下での触媒の構造安定性についての包括的な理解を与えます。
材料科学では、フラーレン、メタロポルフィリン、その他の複雑な化合物など、多くの複雑な無機および有機金属システムが単結晶法を使用して分析されています。単結晶回折は、多形に関する最近の問題のために、製薬業界でも使用されています。単結晶構造の品質に影響を与える主な要因は、結晶のサイズと規則性です。再結晶は、小分子結晶のこれらの要因を改善するために一般的に使用される手法です。ケンブリッジ構造データベースは、 2019年6月の時点で1,000,000以上の構造が含まれています。これらの構造の99%以上がX線回折によって決定されました。
鉱物学および冶金学

火星の土壌の最初のX線回折ビュー– CheMin分析により、長石、
輝石、
かんらん石などが明らかに
なりました( 2012年10月17日、「ロックネスト」のキュリオシティローバー)。
1920年代以降、X線回折は鉱物や金属の原子の配置を決定するための主要な方法でした。X線結晶学の鉱物学への応用は、1924年にメンツァーによって決定されたガーネットの構造から始まりました。ケイ酸塩の体系的なX線結晶学的研究は1920年代に行われた。この研究は、Si / O比が変化すると、ケイ酸塩結晶がそれらの原子配列に有意な変化を示すことを示しました。Machatschkiは、これらの洞察を、アルミニウムがケイ酸塩のシリコン原子の代わりになる鉱物にまで拡張しました。X線結晶学の冶金学への最初の適用も同様に1920年代半ばに起こりました。 最も注目すべきは、ライナス・ポーリングの合金Mg 2 Sn の構造が、錯イオン結晶の安定性と構造に関する彼の理論につながったことです。
2012年10月17日には、好奇心ローバーの火星「でRocknestは」の最初のX線回折分析を行っ火星の土を。ローバーのCheMinアナライザーの結果は、長石、輝石、かんらん石などのいくつかの鉱物の存在を明らかにし、サンプルの火星の土壌がハワイの火山の「風化した玄武岩質土壌」に類似していることを示唆しました。
初期の有機および小さな生体分子

1945年にドロシークロウフットホジキンによって解決された
ペニシリンの3次元構造
。緑、赤、黄、青の球は、それぞれ炭素、 酸素、 硫黄、
窒素の原子を表してい
ます。白い球は水素を表し
ており、X線分析ではなく数学的に決定されています。
有機化合物の最初の構造であるヘキサメチレンテトラミンは1923年に解決されました。これに続いて、生体膜の重要な成分である長鎖脂肪酸のいくつかの研究が行われました。 1930年代に、2次元の複雑さを持つはるかに大きな分子の構造が解明され始めました。重要な進歩はフタロシアニンの構造であり、ヘム、カムイ、クロロフィルなどの生物学で重要なポルフィリン分子と密接に関連している大きな平面分子です。
生体分子のX線結晶学は、コレステロール(1937)、ペニシリン(1946)、ビタミンB 12(1956)の構造を解明したドロシー・クロウフット・ホジキンとともに始まり、1964年にノーベル化学賞を受賞しました。 1969年、彼女は30年以上にわたって取り組んできたインスリンの構造を解明することに成功しました。
生体高分子結晶学

ミオグロビンの構造の
リボン図。色付きのアルファヘリックスを示してい
ます。このような
タンパク質は、数千の原子を持つ長い線形
分子です。それでも、各原子の相対位置は、X線結晶学による亜原子分解能で決定されています。すべての原子を一度に視覚化することは難しいため、リボンはタンパク質のバックボーンのN末端(青)からC末端(赤)までの大まかな経路を示してい クリスタル(不規則であり、コレステロールよりも大きな数百倍)タンパク質の構造は、構造から始まる、1950年代後半に解決されるようになったマッコウクジラ ミオグロビンにより、サー・ジョン・カウドリKendrew、はそのために彼は、共有にノーベル賞を1962年のマックス・ペルーツとの化学。その成功以来、タンパク質、核酸、その他の生体分子の13万を超えるX線結晶構造が決定されてきた。分析された構造の数で最も近い競合する方法は、核磁気共鳴(NMR)分光法であり、これは10分の1未満しか分解され結晶学は任意の大きな分子の構造を解くことができますが、溶液状態のNMRは比較的小さな分子(70 k Da未満)に制限されます。X線結晶学は、医薬品がそのタンパク質標的とどのように相互作用し、どのような変化がそれを改善する可能性があるかを決定するために日常的に使用されます。しかしながら、内因性膜タンパク質は、それらを単独で可溶化するために界面活性剤または他の変性剤を必要とし、そのような界面活性剤はしばしば結晶化を妨げるため、結晶化が困難なままです。膜タンパク質はゲノムの大きな構成要素であり、イオンチャネルや受容体など、生理学的に非常に重要な多くのタンパク質が含まれています。 ヘリウム極低温学は、タンパク質結晶の放射線損傷を防ぐために使用されます。
サイズスケールの反対側では、比較的小さな分子でさえ、X線結晶学の分解能に課題をもたらす可能性が1991年に海洋生物から分離された抗生物質であるジアゾナミドA(C 40 H 34 Cl 2 N 6 O 6、モル質量765.65 g / mol)に割り当てられた構造は、古典的な構造の証明である合成サンプルによって正しくないことが証明されました。天然物と同一ではありませんでした。ミスが正しい-OH / -NHおよび-NH入れ替え区別するX線結晶学のできないことに起因していた2間違った構造に/ -O-基。しかしながら、計装の進歩により、同様のグループは、最新の単結晶X線回折計を使用して区別することができます。
構造生物学において非常に貴重なツールであるにもかかわらず、タンパク質結晶学は、データの解釈を妨げるその方法論にいくつかの固有の問題を抱えています。結晶化プロセス中に形成される結晶格子には、結晶内に密に対称的に詰め込まれた多数の精製タンパク質が含まれています。これまで知られていなかったタンパク質を探すとき、結晶格子内のその形状と境界を理解することは困難な場合がタンパク質は通常、より小さなサブユニットで構成されており、サブユニットを区別して実際のタンパク質を特定する作業は、経験豊富な結晶学者にとっても困難な場合が結晶化中に発生する非生物学的界面は、結晶充填接触(または単に結晶接触)として知られており、結晶学的手段では区別できません。新しいタンパク質構造がX線結晶学によって解明され、タンパク質データバンクに寄託された場合、その著者は、機能的で生物学的に関連するタンパク質を構成する「生物学的集合体」を指定するよう求められます。ただし、エラー、データの欠落、およびデータの送信中の不正確な注釈は、あいまいな構造を引き起こし、データベースの信頼性を損ないます。誤った注釈のみの場合のエラー率は、6.6%または約15%以上であると報告されており、堆積された構造の数を考慮すると、おそらく重要なサイズです。この「インターフェース分類問題」は、通常、計算アプローチによって取り組まれ、構造バイオインフォマティクスで認識されている主題になっています。
散乱技術
X線散乱技術
弾性散乱と非弾性散乱
X線結晶学は弾性散乱の一形態です。出て行くX線は入ってくるX線と同じエネルギー、したがって同じ波長を持っていますが、方向が変わっているだけです。対照的に、非弾性散乱は、エネルギーが入射X線から結晶に伝達されるときに発生します。たとえば、内殻電子をより高いエネルギーレベルに励起することによって発生します。このような非弾性散乱は、発信ビームのエネルギーを減少させます(または波長を増加させます)。非弾性散乱は、このような物質の励起を調べるのに役立ちますが、X線結晶学の目標である物質内の散乱体の分布を決定するのには役立ちません。
X線の波長範囲は10〜0.01ナノメートルです。結晶学に使用される典型的な波長は 1Å(0.1 nm)であり、これは共有化学結合と単一原子の半径のスケールです。(例えば、より長い波長の光子紫外線 放射は)原子位置を決定するのに十分な解像度を持っていないであろう。もう一方の極端な例として、ガンマ線などの短波長の光子は、大量に生成するのが難しく、焦点を合わせるのが難しく、物質との相互作用が強すぎて、粒子と反粒子のペアが生成されます。したがって、X線は、電磁放射の散乱から原子分解能構造を決定する際の波長の「スイートスポット」です。
その他のX線技術
単結晶回折以外の他の形態の弾性X線散乱には、粉末回折、小角X線散乱(SAXS)、およびロザリンドフランクリンが二重らせん構造を決定する際に使用したいくつかのタイプのX線繊維回折が含まれます。DNA。一般に、単結晶X線回折は、これらの他の手法よりも多くの構造情報を提供します。ただし、十分に大きくて規則的な結晶が必要であり、常に利用できるとは限りません。
これらの散乱法は一般に単色X線を使用しますが、これはわずかな偏差で単一波長に制限されます。広域スペクトルのX線(つまり、異なる波長のX線のブレンド)を使用して、ラウエ法として知られる手法であるX線回折を実行することもできます。これは、X線回折の最初の発見で使用された方法です。ラウエ散乱は、X線ビームへの短時間の曝露で多くの構造情報を提供するため、非常に高速なイベントの構造研究で使用されます(時間分解結晶学)。ただし、結晶の完全な原子構造を決定するための単色散乱ほど適ししたがって、比較的単純な原子配列を持つ結晶でより適切に機能します。
ラウエ後方反射モードは、広域スペクトル源から後方に散乱されたX線を記録します。これは、サンプルが厚すぎてX線が透過できない場合に役立ちます。結晶内の回折面は、回折面の法線が入射ビームと回折ビームの間の角度を二等分することを知ることによって決定されます。Greningerチャートを使用することができる背面反射ラウエ写真を解釈します。
電子および中性子回折
電子や中性子などの他の粒子を使用して、回折パターンを生成することができます。電子、中性子、およびX線散乱は異なる物理的プロセスに基づいていますが、結果として得られる回折パターンは、同じコヒーレント回折イメージング技術を使用して分析されます。
以下に示すように、結晶内の電子密度と回折パターンは、単純な数学的方法であるフーリエ変換によって関連付けられます。これにより、密度をパターンから比較的簡単に計算できます。ただし、これは、散乱が弱い場合、つまり、散乱ビームが入射ビームよりもはるかに弱い場合にのみ機能します。弱く散乱されたビームは、2回目の散乱イベントを受けることなく結晶の残りの部分を通過します。このような再散乱波は「二次散乱」と呼ばれ、分析の妨げになります。十分に厚い結晶は二次散乱を生成しますが、X線は電子と比較的弱く相互作用するため、これは一般に重要な問題ではありません。対照的に、電子ビームは、比較的薄い結晶(> 100 nm)でも強い二次散乱を生成する可能性がこの厚さは多くのウイルスの直径に対応するため、有望な方向は、ウイルスキャプシドや分子機械などの孤立した高分子集合体の電子回折であり、これは極低温電子顕微鏡で実行できます。さらに、電子と物質の強い相互作用(X線の約1000倍)により、非常に小さな体積の原子構造を決定することができます。電子結晶学の応用分野は、有機薄膜上の膜タンパク質のような生体分子から、(ナノ結晶)金属間化合物やゼオライトの複雑な構造にまで及びます。
中性子回折は構造決定のための優れた方法ですが、十分な量の強力な単色中性子ビームを得るのは困難でした。核破砕によって中性子を生成する線源がますます利用可能になっているが、伝統的に原子炉が使用されてきた。中性子は帯電していないため、電子からではなく原子核からはるかに容易に散乱します。したがって、中性子散乱は、X線回折では本質的に見えない電子、特に水素の少ない軽い原子の位置を観察するのに非常に役立ちます。中性子散乱はまた、溶媒は通常の比率調整することによって不可視にすることができることは注目すべき性質有する水、H 2 O、および重水、D 2 Oを
メソッド
単結晶X線回折の概要

X線結晶学によって分子の構造を解くためのワークフロー。
X線結晶学の最も古くて最も正確な方法は単結晶X線回折であり、X線のビームが単結晶に衝突して散乱ビームを生成します。それらがフィルムまたは他の検出器に着地すると、これらのビームはスポットの回折パターンを作ります。これらのビームの強度と角度は、結晶が徐々に回転するときに記録されます。各スポットが呼び出され、反射が結晶内の等間隔の平面の一組からのX線の反射に対応するので、。十分な純度と規則性のある単結晶の場合、X線回折データにより、平均化学結合長と角度をそれぞれ数千オングストローム以内と数十分の一度以内に決定できます。結晶内の原子は静的ではありませんが、通常は10分の数オングストローム未満で平均位置を中心に振動します。X線結晶学はこれらの振動のサイズを測定することを可能にします。
手順
単結晶X線結晶学の技術には3つの基本的なステップが最初の、そしてしばしば最も難しいステップは、研究中の材料の適切な結晶を取得することです。結晶は十分に大きく(通常、すべての寸法で0.1 mmより大きく)、組成が純粋で、構造が規則的であり、亀裂や双晶などの重大な内部欠陥がない必要が
2番目のステップでは、結晶を通常は単一波長の強力なX線ビーム(単色X線)に配置し、規則的な反射パターンを生成します。回折されたX線の角度と強度が測定され、各化合物は固有の回折パターンを持っています。結晶が徐々に回転すると、以前の反射が消え、新しい反射が現れます。すべてのスポットの強度は、結晶のすべての方向で記録されます。複数のデータセットを収集する必要がある場合が各セットは、結晶の完全な回転の半分よりわずかに多くをカバーし、通常は数万の反射を含みます。
3番目のステップでは、これらのデータを補完的な化学情報と計算的に組み合わせて、結晶内の原子の配置のモデルを作成および改良します。原子配列の最終的な洗練されたモデル(現在は結晶構造と呼ばれています)は、通常、公開データベースに保存されています。
制限事項
参照:
解像度(電子密度)
結晶の繰り返し単位であるユニットセルが大きく複雑になると、X線結晶学によって提供される原子レベルの画像は、特定の数の観測された反射に対して十分に解像されなくなります(より「ぼやけた」)。X線結晶学の2つの限定的なケース、「小分子」(連続的な無機固体を含む)と「高分子」結晶学がしばしば識別されます。小分子結晶学は通常、非対称単位に100個未満の原子を含む結晶を含みます。このような結晶構造は通常、非常によく分解されているため、原子は電子密度の孤立した「ブロブ」として識別できます。対照的に、高分子結晶学はしばしばユニットセル内の数万の原子を含みます。このような結晶構造は、一般に、あまりよく解像されていません(より「塗りつぶされている」)。原子と化学結合は、孤立した原子としてではなく、電子密度のチューブとして表示されます。一般に、小分子は高分子よりも結晶化が容易です。しかし、X線結晶学は、結晶学的イメージングと技術の改善により、数十万の原子を含むウイルスやタンパク質でも可能であることが証明されています。通常、X線結晶学はサンプルが結晶形である場合にのみ実行できますが、非結晶形のサンプルをサンプリングするための新しい研究が行われています。
結晶
結晶化、
再結晶(化学)§単一完全結晶(X線分析用)、および
タンパク質結晶化

顕微鏡で見たタンパク質の結晶
。X線結晶学で使用される結晶は、直径が1ミリメートル未満の場合が
結晶学は、不純または不規則な結晶の無秩序を特徴づけるために使用できますが、結晶学は一般に、原子の複雑な配列の構造を解決するために高い規則性の純粋な結晶を必要とします。純粋で規則的な結晶は、金属、鉱物、その他の巨視的な材料のサンプルなど、天然または合成の材料から得られる場合がこのような結晶の規則性は、高分子結晶アニーリング やその他の方法で改善できる場合がしかし、多くの場合、回折品質の結晶を得ることが、その原子分解能構造を解く上での主な障壁です。
小分子結晶学と高分子結晶学は、回折品質の結晶を製造するために使用できる技術の範囲が異なります。小分子は一般にコンフォメーションの自由度がほとんどなく、化学蒸着や再結晶などのさまざまな方法で結晶化できます。対照的に、高分子は一般に多くの自由度を持っており、安定した構造を維持するためにそれらの結晶化を実行する必要がたとえば、タンパク質やより大きなRNA分子は、それらの三次構造が展開されている場合は結晶化できません。したがって、結晶化条件の範囲は、そのような分子が折りたたまれたままである溶液条件に制限されます。

結晶を調製する3つの方法、A:ハンギングドロップ。B:シッティングドロップ。C:マイクロダイアリシス
タンパク質の結晶は、ほとんどの場合、溶液中で成長します。最も一般的なアプローチは、その構成分子の溶解度を非常にゆっくりと下げることです。これが速すぎると、分子が溶液から沈殿し、容器の底に役に立たないほこりやアモルファスゲルが形成されます。溶液中での結晶成長は、微視的な結晶子(おそらく100分子しかない)の核形成と、それに続く理想的には回折品質の結晶へのその結晶子の成長という2つのステップによって特徴付けられます。 最初のステップ(核形成)に有利な溶液条件は、2番目のステップ(その後の成長)に有利な条件と常に同じであるとは限りません。結晶学者の目標は、単一の大きな結晶の開発に有利な溶液条件を特定することです。これは、大きな結晶が分子の解像度を向上させるためです。その結果、溶液条件は最初のステップ(核形成)を嫌うが、2番目のステップ(成長)を好むはずなので、液滴ごとに1つの大きな結晶だけが形成されます。核形成があまりにも好まれると、1つの大きな結晶ではなく、小さな結晶子のシャワーが液滴内に形成されます。あまり好まれないと、結晶はまったく形成されません。他のアプローチは、油の下でタンパク質を結晶化することを含みます。そこでは、タンパク質水溶液が液体油の下で分配され、水が油の層を通して蒸発します。油が異なれば蒸発透過性も異なるため、異なる知覚剤/タンパク質混合物からの濃度率に変化が生じます。
秩序だった結晶の核形成または成長のための良好な条件を予測することは非常に困難です。実際には、好ましい状態はスクリーニングによって特定されます。分子の非常に大きなバッチが準備され、多種多様な結晶化溶液がテストされます。成功するものを見つける前に、一般に数百、さらには数千の解条件が試されます。さまざまな条件で、1つまたは複数の物理的メカニズムを使用して分子の溶解度を下げることができます。たとえば、pHを変更するもの、ホフマイスターシリーズの塩または溶液の誘電率を下げる化学物質を含むもの、エントロピー効果によって分子を溶液から追い出すポリエチレングリコールなどの大きなポリマーを含むものが結晶化を促進するためにいくつかの温度を試すこと、または溶液が過飽和になるように徐々に温度を下げることも一般的です。これらの方法は、結晶化する分子を高濃度で使用するため、大量の標的分子を必要とします。このような大量(ミリグラム)の結晶化グレードのタンパク質を得るのは難しいため、100ナノリットルのオーダーの結晶化トライアルドロップを正確に分配できるロボットが開発されました。これは、手作業で設定された結晶化試験(1マイクロリットルのオーダー)と比較した場合、実験ごとに使用されるタンパク質が10分の1であることを意味します。
結晶化を阻害または損なういくつかの要因が知られています。成長する結晶は一般に一定の温度に保たれ、結晶化を妨げる可能性のある衝撃や振動から保護されます。分子内または結晶化溶液中の不純物は、結晶化に対して非現実的であることがよく分子のコンフォメーションの柔軟性も、エントロピーのために結晶化の可能性を低くする傾向が通常のらせんに自己集合する傾向のある分子は、結晶に集合することを望まないことがよく結晶は双晶によって傷つく可能性がこれは、ユニットセルが複数の方向で等しく有利にパックできる場合に発生する可能性が計算方法の最近の進歩により、いくつかの双晶の構造を解くことができるかもしれませんが。ターゲット分子の結晶化に失敗した場合、結晶学者は分子のわずかに変更されたバージョンで再試行する場合が分子特性のわずかな変化でさえ、結晶化挙動に大きな違いをもたらす可能性が
データ収集
クリスタルの取り付け

メディアを再生する
4円カッパゴニオメーターで可能な5つの動きを示すアニメーション。4つの角度φ、κ、ω、および2θのそれぞれの周りの回転は、X線ビーム内に結晶を残しますが、結晶の向きを変更します。検出器(赤いボックス)は、結晶に近づけたり遠ざけたりすることができ、より高い解像度のデータを取得したり(近ければ)、ブラッグピークをよりよく識別できます(遠い場合)。
結晶は、X線ビームに保持されて回転できるように測定用に取り付けられています。取り付けにはいくつかの方法が過去には、結晶は結晶化溶液(母液)とともにガラスキャピラリーにロードされていました。今日では、小分子の結晶は通常、ナイロンまたはプラスチックでできており、中実の棒に取り付けられているガラス繊維またはループに油または接着剤で取り付けられています。タンパク質の結晶はループですくい上げられ、液体窒素で瞬間冷凍されます。この凍結は、X線の放射損傷、および熱運動によるブラッグピークのノイズ(デバイ-ワラー効果)を低減します。ただし、未処理のタンパク質結晶は、瞬間冷凍するとひびが入ることがよくしたがって、それらは通常、凍結する前に凍結防止剤溶液に事前に浸されています。残念ながら、この事前浸漬はそれ自体が結晶に亀裂を生じさせ、結晶学のためにそれを台無しにする可能性が一般的に、成功した低温状態は試行錯誤によって識別されます。
キャピラリーまたはループはゴニオメーターに取り付けられているため、X線ビーム内に正確に配置して回転させることができます。結晶とビームの両方が非常に小さいことが多いため、結晶はビーム内で約25マイクロメートルの精度で中心に配置する必要がこれは、結晶に焦点を合わせたカメラによって支援されます。最も一般的なタイプのゴニオメーターは「カッパゴニオメーター」で、3つの回転角を提供します。ω角はビームに垂直な軸を中心に回転します。ω軸に対して約50°の軸を中心としたκ角。そして最後に、ループ/キャピラリー軸の周りのφ角度。κ角がゼロの場合、ω軸とφ軸が整列します。κ回転により、結晶が取り付けられているアームを結晶学者に向けて振り出すことができるため、結晶を簡単に取り付けることができます。データ収集中に実行される振動(後述)には、ω軸のみが含まれます。古いタイプのゴニオメーターは4円ゴニオメーターであり、その親戚は6円ゴニオメーターなどです。
X線源
回折計、
シンクロトロン光源、および
自由電子レーザー
回転陽極
小規模の結晶学は、通常はイメージプレート検出器と組み合わせた局所X線管源を使用して行うことができます。これらには、比較的安価で保守が容易であるという利点があり、サンプルの迅速なスクリーニングと収集が可能です。ただし、生成される光の波長は、さまざまなアノード材料の可用性によって制限されます。さらに、強度は、アノードの溶融を回避するために適用される電力および利用可能な冷却能力によって制限されます。このようなシステムでは、電子は陰極から沸騰し、約50kVの強い電位によって加速され ます。高速に達すると、電子は金属板と衝突し、制動放射と、金属の内殻電子の励起に対応するいくつかの強いスペクトル線を放出します。使用される最も一般的な金属である銅の高いによるクール容易に保つことができ、熱伝導性、かつ強い生成KをαとK β線を。K β線は、しばしば薄い(〜10μm)をニッケル箔で抑制されます。最も単純で最も安価な種類の密閉型X線管は、固定陽極(クルックス管)を備えており、約 2kWの電子ビーム出力で動作します。より高価な品種には、約14kWの電子ビーム電力で動作する回転陽極タイプの光源が
X線は通常、(X線フィルターを使用して)単一波長にフィルター処理され(単色化)、結晶に当たる前に単一方向にコリメートされます。フィルタリングは、データ分析を簡素化するだけでなく、有用な情報を提供することなく結晶を劣化させる放射線を除去します。コリメーションは、コリメータ(基本的には長いチューブ)または緩やかに湾曲したミラーの巧妙な配置のいずれかを使用して行われます。ミラーシステムは、小さな結晶(0.3 mm未満)または大きなユニットセル(150Å以上)に適しています。
回転アノードは、量子井戸レーザーの品質管理のための大型InGaAsP薄膜ウェーハの迅速な(リアルタイム生産)スクリーニングのためのX線のパワーを実証した最初の実験 で、Joanna(Joka)MariaVandenbergによって使用されました。。
マイクロフォーカスチューブ
より最近の開発はマイクロフォーカスチューブであり、これは回転陽極源と少なくとも同じくらい高いビームフラックス(コリメーション後)を供給することができますが、数キロワットを必要とするのではなく、数十または数百ワットのビームパワーしか必要としません。
放射光
放射光源は、地球上で最も明るい光源の一部であり、X線結晶学者が利用できる最も強力なツールの一部です。シンクロトロンと呼ばれる大型の機械で生成されたX線ビームは、荷電粒子(多くの場合電子)をほぼ光速まで加速し、磁場を使用して(ほぼ)円形のループに閉じ込めます。
シンクロトロンは一般的に国の施設であり、それぞれにデータが中断することなく収集されるいくつかの専用ビームラインがシンクロトロンはもともと、素粒子と宇宙現象を研究する高エネルギー物理学者が使用するために設計されました。各シンクロトロンの最大の構成要素は、その電子蓄積リングです。このリングは実際には完全な円ではなく、多面的なポリゴンです。ポリゴンまたはセクターの各コーナーで、正確に位置合わせされた磁石が電子の流れを曲げます。電子の経路が曲がると、X線の形でエネルギーのバーストを放出します。
シンクロトロン放射光の使用には、X線結晶学に関する特定の要件が頻繁に強い電離放射線は、サンプル、特に高分子結晶に放射線損傷を引き起こす可能性が低温結晶学は、液体窒素温度(〜100 K)で結晶を凍結することにより、放射線による損傷からサンプルを保護します。しかしながら、シンクロトロン放射はしばしばユーザーが選択可能な波長の利点を持っており、異常信号を最大化する異常散乱実験を可能にします。これは、単一波長異常分散(SAD)や多波長異常分散(MAD)などの実験では重要です。
自由電子レーザー
自由電子レーザーは、X線結晶学で使用するために開発されました。これらは現在利用可能な最も明るいX線源です。X線はフェムト秒バーストで送られます。線源の強度は、原子分解能の回折パターンが結晶に対して分解できるようなものであり、そうでなければ収集するには小さすぎます。ただし、強力な光源はサンプルも破壊するため、複数の結晶を発射する必要が各結晶はビーム内でランダムに配向しているため、完全なデータセットを取得するには、数十万の個別の回折画像を収集する必要がこの方法であるシリアルフェムト秒結晶学は、多くのタンパク質結晶構造の構造を解くのに使用されており、シンクロトロン源から収集された同等の構造との違いに気付くことが
反射を記録する

結晶化した酵素のX線回折パターン。スポットのパターン(反射)と各スポットの相対強度(強度)を使用して、酵素の構造を決定できます。
結晶が取り付けられ、X線の強いビームにさらされると、結晶の背後にあるスクリーンで観察できるスポットまたは反射のパターンにX線が散乱します。コンパクトディスクにレーザーポインターを当てると、同様のパターンが見られる場合がこれらのスポットの相対強度は、結晶内の分子の配置を原子の詳細で決定するための情報を提供します。これらの反射の強度は、写真フィルム、エリア検出器(ピクセル検出器など)、または電荷結合デバイス(CCD)イメージセンサーを使用して記録できます。小さな角度のピークは低解像度のデータに対応し、高い角度のピークは高解像度のデータを表します。したがって、構造の最終的な解像度の上限は、最初の数枚の画像から決定できます。ピーク幅で観察されるように、結晶のモザイク性およびその全体的な無秩序など、回折品質のいくつかの尺度をこの時点で決定することができます。構造を解くのに適さない結晶のいくつかの病状も、この時点で迅速に診断することができます。
スポットの1つの画像は、結晶全体を再構成するには不十分です。これは、完全なフーリエ変換のごく一部を表しています。必要なすべての情報を収集するには、結晶を180°ずつ段階的に回転させ、すべての段階で画像を記録する必要が実際には、エワルド球の曲率のために、逆格子空間をカバーするために180°よりわずかに多くが必要です。ただし、結晶の対称性が高い場合は、90°や45°などの狭い角度範囲が記録される場合が回転軸に近い逆格子空間に「死角」が発生しないように、回転軸は少なくとも1回は変更する必要が逆格子空間のより広い領域を捕らえるために、結晶をわずかに(0.5〜2°)揺り動かすのが通例です。
特定のフェーズ方法では、複数のデータセットが必要になる場合がたとえば、多波長異常分散位相調整では、入射X線放射の少なくとも3つ(冗長性のために通常は4つ)の波長で散乱を記録する必要が単結晶は、放射線による損傷のために、1つのデータセットの収集中に劣化しすぎる可能性がこのような場合、複数の結晶に関するデータセットを取得する必要が
データ分析
結晶対称性、ユニットセル、および画像スケーリング
空間群
それぞれが異なる結晶方位に対応する、記録された一連の2次元回折パターンは、電子密度の3次元モデルに変換されます。変換では、フーリエ変換の数学的手法を使用します。これについては、以下で説明します。各スポットは、電子密度のさまざまなタイプの変動に対応します。結晶学者は、どのバリエーションがどのスポットに対応するか(インデックス付け)、異なる画像内のスポットの相対強度(マージとスケーリング)、およびバリエーションを組み合わせて総電子密度を生成する方法(フェーズ)を決定する必要が
データ処理は、反射のインデックス付けから始まります。これは、ユニットセルの寸法と、どの画像ピークが逆格子空間のどの位置に対応するかを特定することを意味します。インデックス付けの副産物は、結晶の対称性、つまりその空間群を決定することです。一部の空間群は最初から削除できます。たとえば、反射対称性はキラル分子では観察できません。したがって、ほとんどの場合キラルであるタンパク質分子には、230個の可能な65個の空間群のみが許可されます。インデックス作成は通常、自動インデックス作成ルーチンを使用して実行されます。対称性を割り当てた後、データは統合されます。これにより、数千の反射を含む数百の画像が1つのファイルに変換されます。このファイルは、(少なくとも)各反射のミラー指数のレコードと各反射の強度で構成されます(この状態では、ファイルにはエラー推定値も含まれることがよくあります)および部分性の測定(特定の反射のどの部分がその画像に記録されたか))。
完全なデータセットは、結晶のさまざまな方向で撮影された何百もの個別の画像で構成されている場合が最初のステップは、これらのさまざまな画像をマージしてスケーリングすることです。つまり、2つ以上の画像に表示されるピークを識別し(マージ)、一貫した強度スケールを持つように相対画像をスケーリングします。ピークの相対強度が構造を決定するための重要な情報であるため、強度スケールの最適化は重要です。結晶学的データ収集の反復技術と結晶性材料のしばしば高い対称性により、回折計は多くの対称性に相当する反射を複数回記録します。これは、対称関連計算可能R-因子、対称等価反射の測定強度であるか類似に基づいて信頼性指標、したがって、データの品質を評価します。
初期フェーズ
位相問題
回折実験から収集されたデータは、結晶格子の逆空間表現です。各回折「スポット」の位置は、ユニットセルのサイズと形状、および結晶内の固有の対称性によって決まります。各回折「スポット」の強度が記録され、この強度は構造因子の 振幅の2乗に比例します。構造因子である複素数の両方に関連する情報を含む振幅および位相の波動。解釈可能な電子密度マップを取得するには、振幅と位相の両方を知る必要があります(電子密度マップにより、結晶学者は分子の開始モデルを構築できます)。回折実験中に位相を直接記録することはできません。これは位相問題として知られています。初期段階の見積もりは、さまざまな方法で取得できます。
アブイニシオフェージングまたは直接法 –これは通常、小分子(<1000非水素原子)に最適な方法であり、小タンパク質の相問題を解決するために使用されています。データの解像度が1.4Å(140pm)よりも優れている場合は 、特定の反射グループ間の既知の位相関係を利用することにより、直接的な方法を使用して位相情報を取得できます。
分子置換 –関連する構造がわかっている場合は、分子置換の検索モデルとして使用して、ユニットセル内の分子の方向と位置を決定できます。このようにして得られた位相は、電子密度マップを生成するために使用できます。
異常なX線散乱( MADまたはSADフェージング)– X線の波長は、吸収端を超えてスキャンされる場合があります[次のように定義されている場合?]原子の、既知の方法で散乱を変更します。3つの異なる波長(吸収端のはるか下、はるか上、中央)で反射の完全なセットを記録することにより、異常に回折する原子の下部構造、したがって分子全体の構造を解くことができます。異常散乱原子をタンパク質に組み込む最も一般的な方法は、セレン原子を含むセレノメチオニンが豊富な培地でメチオニン栄養要求性(メチオニンを合成できない宿主)でタンパク質を発現させることです。次に、多波長異常分散(MAD)実験を吸収端の周りで実行できます。これにより、タンパク質内のメチオニン残基の位置が得られ、初期段階が提供されます。
重原子法(多重同形置換法)–電子密度の高い金属原子を結晶に導入できる場合は、直接法またはパターソン空間法を使用して、それらの位置を決定し、初期相を取得できます。このような重原子は、結晶を重原子含有溶液に浸すことによって、または共結晶化(重原子の存在下で結晶を成長させること)によって導入することができる。多波長異常分散位相法と同様に、散乱振幅の変化を解釈して位相を生成することができます。これはタンパク質の結晶構造を解明するための独自の方法ですが、セレノメチオニンによる多波長異常分散法に大きく取って代わられています。
モデル構築とフェーズの改良

超高解像度(0.91Å)での結晶構造の電子密度内での共有結合のスティック図を使用した、タンパク質のアルファヘリックスの構造。密度の輪郭は灰色、らせん骨格は白、側鎖はシアン、O原子は赤、N原子は青、水素結合は緑の点線で示されています。

タンパク質(黄色)の結合部位に結合したリガンド(オレンジ)の電子密度(青)の3D描写。
電子密度は実験データから得られ、配位子はこの電子密度にモデル化されます。
分子モデリング
初期段階を取得したら、初期モデルを構築できます。モデル内の原子位置とそれぞれのデバイ-ワラー因子(または原子の熱運動を説明するB因子)は、観測された回折データに合うように調整でき、理想的にはより良い相のセットを生成します。次に、新しいモデルを新しい電子密度マップに適合させることができ、一連の改良が実行されます。この相互作用プロセスは、回折データとモデル間の相関が最大になるまで続きます。一致は、次のように定義されるRファクターによって測定されます。 = ∑ すべての反射 | obs − 計算 | ∑
すべての反射 | obs | {R = { frac { sum _ { text {all Reflections}} left | F _ { text {obs}}-F _ { text {calc}} right |} { sum _ { text {all Reflections}} left | F _ { text {obs}} right |}}、}
ここで、Fは構造因子です。同様の品質基準はRフリーです。これは、構造の改良に含まれなかった反射のサブセット(〜10%)から計算されます。両方のR係数は、データの解像度に依存します。経験則として、R freeは、およそオングストローム単位の解像度を10で割った値である必要がしたがって、2Åの分解能を持つデータセットは、最終的なRフリー〜0.2を生成するはずです。立体化学、水素結合、結合長と角度の分布などの化学結合機能は、モデル品質の補完的な指標です。位相バイアスは、このような反復モデル構築において深刻な問題です。マップの省略は、これをチェックするために使用される一般的な手法です。
非対称ユニット内のすべての原子を観察できるとは限りません。多くの場合、結晶学的無秩序は電子密度マップを塗りつぶします。水素などの弱く散乱する原子は、日常的には見えません。たとえば、タンパク質の側鎖に複数(<4)の許可されたコンフォメーションがある場合、単一の原子が電子密度マップに複数回出現する可能性もさらに他の場合には、結晶学者は、分子について推定された共有結合構造が不正確であるか、または変化したことを検出する可能性がある。例えば、タンパク質は、結晶化の前に検出されなかった切断または翻訳後修飾を受ける可能性が
障害
結晶学的障害
結晶構造の精密化における一般的な課題は、結晶学的無秩序に起因します。障害は多くの形態をとることができますが、一般的には2つ以上の種またはコンフォメーションの共存を伴います。障害を認識できないと、解釈に欠陥が生じます。障害の不適切なモデリングからの落とし穴は、結合ストレッチ異性の割引された仮説によって示されます。障害は、コンポーネントの相対的な母集団(多くの場合2つのみ)とそれらのアイデンティティに関してモデル化されます。大きな分子とイオンの構造では、溶媒と対イオンが無秩序になることがよく
応用計算データ分析
粉末X線回折データ分析のための計算方法の使用は現在一般化されています。これは通常、実験データをモデル構造のシミュレートされた回折図と比較し、機器のパラメーターを考慮に入れ、最小二乗ベースの最小化アルゴリズムを使用してモデルの構造または微細構造パラメーターを改良します。相の同定および構造精密化を可能にする最も利用可能なツールは、に基づいてリートベルト法、 それらの一部であるようFullProfスイートなどのオープンとフリーソフトウェア、 Jana2006、 MAUD、 Rietan、 GSAS、など、Diffrac.Suite TOPAS、 Match!、などの商用ライセンスで利用できるものもこれらのツールのほとんどは、Le Bailリファインメント(プロファイルマッチングとも呼ばれます)、つまり、結晶構造自体を考慮せずに、ブラッグピーク位置とピークプロファイルに基づいてセルパラメータをリファインします。最近のツールでは、FullProf Suiteに含まれるFAULTSプログラムなど、構造データと微細構造データの両方を改良できます。これにより、平面欠陥(たとえば、積層欠陥、双晶、連晶)のある構造を精密化できます。
構造物の堆積
分子の構造のモデルが完成すると、ケンブリッジ構造データベース(小分子の場合)、無機結晶構造データベース(ICSD)(無機化合物の場合)、タンパク質データバンク(タンパク質データバンク)などの結晶学的データベースに保存されることがよくタンパク質および場合によっては核酸の場合)。医学的に関連するタンパク質を結晶化するために民間の商業ベンチャーで得られた多くの構造は、公的な結晶学データベースに寄託され
回折理論
回折および
ブラッグ回折の動力学理論
X線結晶学の主な目標は、結晶全体の電子密度f(r)を決定することです。ここで、rは結晶内の3次元位置ベクトルを表します。これを行うには、X線散乱を使用してフーリエ変換F(q)に関するデータを収集します。これは数学的に反転され、式を使用して実空間で定義された密度を取得します。 (( NS)。= 1(( 2
π)。 3 ∫ (( NS)。 e I ⋅ NS、
{f( mathbf {r})= { frac {1} { left(2 pi right)^ {3}}} int F( mathbf {q})e ^ { mathrm { i} mathbf {q} cdot mathbf {r}} mathrm {d} mathbf {q}、}
ここで、積分はqのすべての値に適用されます。3次元の実数ベクトルqは、逆格子空間内の点、つまり、qが指す方向に移動するときの電子密度の特定の振動を表します。qの長さはに対応します2 π
{2 pi}
振動の波長で割った値。フーリエ変換に対応する式を以下で使用します (( NS)。 = ∫ (( NS)。e −
I ⋅ NS、
{F( mathbf {q})= int f( mathbf {r}) mathrm {e} ^ {- mathrm {i} mathbf {q} cdot mathbf {r}} mathrm {d} mathbf {r}、}
ここで、積分は、結晶内の位置ベクトルrのすべての可能な値にわたって合計されます。
フーリエ変換F(q)は一般に複素数であるため、大きさは次のようになります。F(q)| および式によって関連付けられる位相 φ(q) (( NS)。 = | ((NS
)。| e I ϕ((NS
)。 {F( mathbf {q})= left | F( mathbf {q}) right | mathrm {e} ^ { mathrm {i} phi( mathbf {q})}。}
X線回折で観察された反射の強度は私たちに大きさを与えます| F(q)| しかし、位相φ(q)ではありません。位相を取得するために、特定の吸収端を超えて波長を変調するか、水銀などの強力な散乱(つまり電子密度の高い)金属原子を追加することにより、散乱に既知の変更を加えた反射のフルセットを収集します。大きさと位相を組み合わせると、完全なフーリエ変換F(q)が得られます。これを反転して、電子密度f(r)を得ることができます。
多くの場合、結晶は完全に周期的であると理想化されています。その理想的なケースでは、原子は完全な格子上に配置され、電子密度は完全に周期的であり、qが逆格子(いわゆるブラッグピーク)に属する場合を除いて、フーリエ変換F(q)はゼロです。ただし、実際には、結晶は完全に周期的ではありません。原子はその平均位置を中心に振動し、モザイク性、転位、さまざまな点欠陥、結晶化分子のコンフォメーションの不均一性など、さまざまなタイプの無秩序が存在する可能性がしたがって、ブラッグピークの幅は有限であり、ブラッグピークの間にある散乱X線の連続体であるかなりの散漫散乱が存在する可能性が
ブラッグの法則による直感的な理解
X線回折の直感的な理解は、回折のブラッグモデルから得ることができます。このモデルでは、特定の反射は、通常、結晶格子の原子の中心を通過する、結晶を通過する等間隔のシートのセットに関連付けられています。シートの特定のセットの方向は、その3つのミラー指数(h、k、l)によって識別され、それらの間隔はdによって示されます。ウィリアム・ローレンス・ブラッグは、入ってくるX線が各平面から鏡面反射(鏡のように)散乱されるモデルを提案しました。その仮定から、隣接する平面から散乱されたX線は、平面とX線の間の角度θがX線波長λの整数倍nである光路長差をもたらす場合、建設的に結合します(建設的干渉)。。2sin θ= λ {2d sin theta = n lambda。}
反射は、そのミラー指数(より正確には、その逆格子ベクトル成分)が既知の波長と散乱角2θから識別されたときに指数化されると言われます。このようなインデックス付けにより、ユニットセルのパラメータ、ユニットセルの長さと角度、およびその空間群が得られます。以来、ブラッグの法則は、反射の相対強度を解釈しない、しかし、単位セル内の原子の配列を解くために一般的に不十分です。そのためには、フーリエ変換法を実行する必要が
フーリエ変換としての散乱
入射するX線ビームには偏光があり、ベクトル波として表す必要がただし、簡単にするために、ここではスカラー波として表現します。また、波の時間依存性の複雑さを無視し、波の空間依存性に集中します。平面波は、の波数ベクトル kで表すことができるため、時間t = 0での到来波の強度は次の式で与えられます。 eI k
I ⋅ 。
{A mathrm {e} ^ { mathrm {i} mathbf {k} _ { mathrm {in}} cdot mathbf {r}}。}
サンプル内の位置rに、散乱体の密度f(r)があるとします。これらの散乱体は、入力波の局所振幅にrについての小さなボリュームdV内の散乱体の数を掛けたものに比例する振幅の散乱球面波を生成する必要が
散乱波の振幅 e I k ⋅(( NS)。V {{ text {散乱波の振幅}} = A mathrm {e} ^ { mathrm {i} mathbf {k} cdot mathbf {r}} Sf( mathbf {r}) mathrm {d} V、}
ここで、Sは比例定数です。
散乱波の割合を考慮することの出射波動ベクトルとの休暇Kアウトとでスクリーンに当たるのRスクリーン。エネルギーが失われないため(非弾性散乱ではなく弾性散乱)、波長は波数ベクトルの大きさと同じです。k in | = | kアウト|。光子がrで散乱されてから、rスクリーンで吸収されるまで、光子の位相が変化します。e I k
アウト ⋅ ((画面
− )。 {e ^ {i mathbf {k} _ { text {out}} cdot left( mathbf {r} _ { text {screen}}- mathbf {r} right)}。}
rスクリーンに到達する正味の放射は、結晶全体のすべての散乱波の合計です。 ∫(( NS)。e I
k⋅ eI k
アウト ⋅ ((画面
− )。= eI k アウト ⋅ 画面
∫(( NS)。e I(( k − k アウト )。 ⋅ 、
{AS int mathrm {d} mathbf {r} f( mathbf {r}) mathrm {e} ^ { mathrm {i} mathbf {k} _ { text {in}} cdot mathbf {r}} e ^ {i mathbf {k} _ { text {out}} cdot left( mathbf {r} _ { text {screen}}- mathbf {r} right )} = ASe ^ {i mathbf {k} _ { text {out}} cdot mathbf {r} _ { text {screen}}} int mathrm {d} mathbf {r} f( mathbf {r}) mathrm {e} ^ { mathrm {i} left( mathbf {k} _ { text {in}}- mathbf {k} _ { text {out}} right ) cdot mathbf {r}}、}
これはフーリエ変換として書くことができます eI k アウト ⋅ 画面
∫(( NS)。e −
I ⋅ = eI k
アウト
⋅ 画面 (( NS)。 {AS mathrm {e} ^ { mathrm {i} mathbf {k} _ { text {out}} cdot mathbf {r} _ { text {screen}}} int d mathbf {r} f( mathbf {r}) mathrm {e} ^ {- mathrm {i} mathbf {q} cdot mathbf {r}} = AS mathrm {e} ^ { mathrm {i } mathbf {k} _ { text {out}} cdot mathbf {r} _ { text {screen}}} F( mathbf {q})、}
ここで、Q = kのうち – kはに。測定された反射の強度は、この振幅の2乗になります 2 2
| (( )。 | 2 {A ^ {2} S ^ {2} left | F( mathbf {q}) right | ^ {2}。}
フリーデルとビボエの仲間
逆格子空間の点qに対応するすべての反射に対して、反対の点-qで同じ強度の別の反射がこの反対の反射は、元の反射のフリーデルメイトとして知られています。この対称性は、位置rでの電子密度f(r)が常に実数であるという数学的事実に起因します。上記のように、f(r)はそのフーリエ変換F(q)の逆変換です。ただし、このような逆変換は一般に複素数です。f(r)が実数であることを保証するには、フーリエ変換F(q)は、フリーデルの仲間F(− q)とF(q)が互いに複素共役になるようなものでなければなりません。したがって、F( – qは)と同じ大き有するF(qは)それらが逆の位相を有する、すなわち、φ(Q)= – φ(Q) (( −
NS)。 = | (( − )。| e I ϕ(( − )。= ∗(( NS)。 = | ((NS
)。| e − I ϕ((NS
)。 {F(- mathbf {q})= left | F(- mathbf {q}) right | mathrm {e} ^ { mathrm {i} phi(- mathbf {q}) } = F ^ {*}( mathbf {q})= left | F( mathbf {q}) right | mathrm {e} ^ {- mathrm {i} phi( mathbf {q} )}。}
それらの大きさが等しいことにより、フリーデルの仲間が同じ強度を持つことが保証されます。F | 2。この対称性により、逆格子空間の半分から完全なフーリエ変換を測定できます。たとえば、結晶を360°完全に回転させるのではなく、180°をわずかに超えて回転させることができます。対称性の高い結晶では、さらに多くの反射が同じ強度を持つ場合があります(Bijvoetメイト)。このような場合、測定する必要のある逆格子空間はさらに少なくなる可能性が対称性が高い好ましいケースでは、逆格子空間を完全に探索するために、90°または45°のデータしか必要とされない場合が
フリーデルメイト制約は、逆フーリエ変換の定義から導き出すことができます。 (( NS)。 = ∫(( 2
π)。
3 (( NS)。 e I ⋅ =
∫(( 2
π)。 3 | ((NS
)。| e I ϕ((NS
)。 e I ⋅ 。
{f( mathbf {r})= int { frac {d mathbf {q}} { left(2 pi right)^ {3}}} F( mathbf {q}) mathrm {e} ^ { mathrm {i} mathbf {q} cdot mathbf {r}} = int { frac {d mathbf {q}} { left(2 pi right)^ { 3}}} left | F( mathbf {q}) right | mathrm {e} ^ { mathrm {i} phi( mathbf {q})} mathrm {e} ^ { mathrm { i} mathbf {q} cdot mathbf {r}}。}
以来、オイラーの公式の電子その状態I 、X = COS(X)+ I SIN(X)、逆フーリエ変換は純粋に実数部と純粋に虚部の和に分離することができます (( NS)。 = ∫(( 2
π)。 3 | ((NS
)。| e I(( ϕ+ ⋅ )。 = ∫(( 2
π)。 3 | ((NS
)。| os(( ϕ+ ⋅ )。+ I ∫(( 2
π)。 3 | ((NS
)。 | sin (( ϕ+ ⋅ )。 = I o + I I I 。
{f( mathbf {r})= int { frac {d mathbf {q}} { left(2 pi right)^ {3}}} left | F( mathbf {q }) right | mathrm {e} ^ { mathrm {i} left( phi + mathbf {q} cdot mathbf {r} right)} = int { frac {d mathbf { q}} { left(2 pi right)^ {3}}} left | F( mathbf {q}) right | cos left( phi + mathbf {q} cdot mathbf {r} right)+ i int { frac {d mathbf {q}} { left(2 pi right)^ {3}}} left | F( mathbf {q}) right | sin left( phi + mathbf {q} cdot mathbf {r} right)= I _ { mathrm {cos}} + iI _ { mathrm {sin}}。}
関数F(rは)もしリアルであり、第2の積分場合にのみ、私の罪のすべての値はゼロであるR。同様に、これは、上記の制約が満たされている場合にのみ当てはまります。 I sin =
∫(( 2
π)。 3 | ((NS
)。 | sin (( ϕ+ ⋅ )。 = ∫(( 2
π)。 3 | ((− )。 | sin (( − ϕ − ⋅ )。=− I
sin {I _ { sin} = int { frac {d mathbf {q}} { left(2 pi right)^ {3}}} left | F( mathbf {q}) right | sin left( phi + mathbf {q} cdot mathbf {r} right)= int { frac {d mathbf {q}} { left(2 pi right)^ {3}}} left | F( mathbf {-q}) right | sin left(- phi- mathbf {q} cdot mathbf {r} right)=-I _ { sin }、}
以来、私の罪= -私の罪は、ことを意味し、私の罪は = 0。
エワルド球
エワルド球
各X線回折画像は、エワルド球の構造からわかるように、スライス、つまり逆格子空間の球形スライスのみを表しています。双方KアウトとKで波長が変化していないので、弾性散乱による同じ長さを有します。したがって、それらは逆格子空間の球内の2つの放射状ベクトルとして表すことができます。これは、特定の回折画像でサンプリングされたqの値を示します。入射X線ビームの入射波長にはわずかな広がりがあるため、|の値は F(q)|は、それらの半径に対応する2つの球の間にあるq個のベクトルに対してのみ測定できます。したがって、フーリエ変換データの完全なセットを取得するには、結晶を180°よりわずかに大きく回転させる必要が十分な対称性が存在する場合は、それより低く回転させることも実関数(電子密度など)のフーリエ変換に固有の対称性のため、完全な360°回転は必要ありませんが、特定の解像度内のすべての逆格子空間をカバーするには、180°より「わずかに大きい」必要がエワルド球の曲率。実際には、結晶は少量(0.25–1°)で揺り動かされ、球形のエヴァルトの殻の境界近くに反射が組み込まれます。
パターソン関数
パターソン関数
フーリエ変換のよく知られた結果は、関数f(r)の自己相関c(r)を示す自己相関定理です。 (( NS)。 = ∫(( NS)。 ((+
NS)。 = ∫(( 2
π)。
3 (( NS)。 e I ⋅ {c( mathbf {r})= int d mathbf {x} f( mathbf {x})f( mathbf {x} + mathbf {r})= int { frac {d mathbf {q}} { left(2 pi right)^ {3}}} C( mathbf {q})e ^ {i mathbf {q} cdot mathbf {r}}}
F(q)の大きさの2乗であるフーリエ変換C(q)を持っています (( NS)。 = | (( )。 | 2 {C( mathbf {q})= left | F( mathbf {q}) right | ^ {2}。}
したがって、電子密度の自己相関関数c(r)(パターソン関数としても知られています)は、位相を計算せずに、反射強度から直接計算できます。原則として、これは結晶構造を直接決定するために使用できます。しかし、実際に実現することは困難です。自己相関関数は、結晶内の原子間のベクトルの分布に対応します。したがって、そのユニットセル内のN原子の結晶は 、そのパターソン関数にN(N − 1)個のピークを持つ可能性が強度の測定における不可避のエラー、および原子間ベクトルから原子位置を再構築することの数学的困難さを考えると、この手法は、最も単純な結晶を除いて、構造を解くために使用されることはめったにありません。
クリスタルの利点
原則として、原子構造は、単一分子であっても、非結晶サンプルにX線散乱を適用することで決定できます。ただし、水晶は周期性があるため、はるかに強い信号を提供します。結晶サンプルは定義上周期的です。結晶は、3つの独立した方向に無期限に繰り返される多くのユニットセルで構成されています。このような周期的システムには、ブラッグピークとして知られる逆格子空間内の周期的に繰り返される点に集中するフーリエ変換がブラッグピークは、回折画像で観察された反射スポットに対応します。これらの反射での振幅は散乱体の数Nに比例して増加するため、これらのスポットの観測された強度はN2のように2次関数的に増加するはずです。言い換えれば、結晶を使用すると、個々のユニットセルの弱い散乱が、ノイズの上で観察できるはるかに強力でコヒーレントな反射に集中します。これは建設的な干渉の例です。
液体、粉末、またはアモルファスのサンプルでは、そのサンプル内の分子はランダムな方向にこのようなサンプルは、SAXSで観察されるように、振幅を均一に拡散し、それによって測定された信号強度を低下させる連続フーリエスペクトルを持っています。さらに重要なことに、方向情報が失われます。理論的には可能ですが、このような回転平均データから複雑な非対称分子の原子分解能構造を取得することは実験的に困難です。中間のケースは、サブユニットが少なくとも1つの次元に周期的に配置されるファイバー回折です。
X線結晶学を含むノーベル賞 年 受賞者 賞 理論的根拠 1914年 マックス・フォン・ラウエ
物理
「結晶によるX線の回折の彼の発見のために」 X線分光法の開発における重要なステップ。 1915年 ウィリアムヘンリーブラッグ
物理
「X線による結晶構造の分析における彼らのサービスに対して」
ウィリアム・ローレンス・ブラッグ 1962年 マックス・F・ペルーツ
化学
「球状タンパク質の構造の研究のために」
ジョン・C・ケンドリュー 1962年 ジェームズ・デューイ・ワトソン 薬 「核酸の分子構造と生体物質における情報伝達におけるその重要性に関する彼らの発見に対して」
フランシス・ハリー・コンプトン・クリック
モーリス・ヒュー・フレデリック・ウィルキンス 1964年 ドロシーホジキン
化学
「重要な生化学物質の構造のX線技術による彼女の決定のために」 1972年 スタンフォード・ムーア
化学
「リボヌクレアーゼ分子の活性中心の化学構造と触媒活性の間の関係の理解への彼らの貢献に対して」
ウィリアム・H・スタイン 1976年 ウィリアム・N・リプスコム
化学
「化学結合の問題を明らかにするボランの構造に関する彼の研究に対して」 1985年 ジェロームカール
化学
「結晶構造を決定するための直接的な方法の開発における彼らの卓越した業績に対して」
ハーバート・A・ハウプトマン 1988年 ヨハン・ダイゼンホーファー
化学
「光合成反応中心の三次元構造の決定のために」
ハルトムート・ミシェル
化学
ロベルトフーバー
化学 1997年 ジョンE.ウォーカー
化学
「アデノシン三リン酸(ATP)の合成の根底にある酵素メカニズムの解明のために」 2003年 ロデリック・マキノン
化学
「細胞膜のチャネルに関する発見のためにイオンチャネルの構造的および機構的研究のために」
ピーター・アグレ
「細胞膜のチャネルに関する発見のために水チャネルの発見のために」 2006年 ロジャー・D・コーンバーグ
化学
「真核生物の転写の分子基盤に関する彼の研究に対して」 2009年 アダ・E・ヨナス
化学
「リボソームの構造と機能の研究のために」
トマス・A・スタイツ
ヴェンカトラマンラマクリシュナン 2012年 ブライアンコビルカ
化学
「Gタンパク質共役型受容体の研究用」
アプリケーション
X線回折は、化学、生化学、物理、材料、鉱物学の分野で幅広くさまざまな用途がラウエは1937年に、この技術は「顕微鏡で得られたものを超えて、微細構造を観察する力を1万倍も拡大した」と主張しました。 X線回折は、原子とその電子分布を示す原子レベルの解像度を持つ顕微鏡に類似しています。
X線回折、電子回折、および中性子回折は、原子および分子レベルで、結晶性および非結晶性の物質の構造に関する情報を提供します。さらに、これらの方法は、無機、有機、または生物学のすべての材料の特性の研究に適用できます。結晶の回折研究の重要性と応用の多様性のために、多くのノーベル賞がそのような研究に対して授与されてきました。
薬物の識別
X線回折は、8つのβ-ラクタム(アンピシリンナトリウム、ペニシリンGプロカイン、セファレキシン、アンピシリン三水和物、ベンザチンペニシリン、ベンジルペニシリンナトリウム、セフォタキシムナトリウム、セフトリアキソンナトリウム)、3つのテトラサイクリン(ドキシサイクリン)などの抗生物質の同定に使用されています。塩酸塩、オキシテトラサイクリン脱水物、テトラサイクリン塩酸塩)および2つのマクロライド(アジスロマイシン、エリスロマイシンエストレート)抗生物質。これらの各薬剤には、識別を可能にする独自のX線回折(XRD)パターンが
ナノマテリアル、繊維、ポリマーの特性評価
痕跡証拠の法医学的検査は、ロカールの交換原理に基づいています。これは、「すべての接触が痕跡を残す」ことを示しています。実際には、物質の移動が起こったとしても、移動量が非常に少ないため、検出できない場合が
XRDは、ナノマテリアル研究の進歩におけるその役割を証明しています。これは主要な特性評価ツールの1つであり、粉末 と薄膜の両方の形態のさまざまなナノ材料の構造特性に関する情報を提供します。
繊維は、結晶性物質と非晶性物質の混合物です。したがって、結晶度の測定は、X線回折法を使用した繊維の特性評価に役立つデータを提供します。X線回折を使用して、椅子に見つかった「結晶性」の堆積物を特定したことが報告されています。堆積物はアモルファスであることが見出されたが、存在する回折パターンはポリメチルメタクリレートのそれと一致した。熱分解 質量分析は、後に堆積物をボイン結晶パラメーターのポリメチルシアノアクリルオンとして同定しました。
骨の調査
骨の加熱または燃焼は、XRD技術を使用して検出できる骨ミネラルの認識可能な変化を引き起こします。500°C以上で加熱してから最初の15分間で、骨の結晶が変化し始めました。高温では、骨の結晶の厚さと形状は安定しているように見えますが、サンプルを低温または短時間で加熱すると、XRDトレースは結晶パラメーターの極端な変化を示しました。
集積回路
X線回折は、集積回路の複雑な構造を調査する方法として実証されています。
も参照してください
ビーバーズ–リプソンストリップ
ブラッグ回折
結晶学データベース
結晶点群
差密度マップ
電子線回折
エネルギー分散型X線回折
フラックパラメータ
ヘンダーソン制限
世界結晶年
ジョン・デスモンド・ベルナル
多極密度形式
中性子回折
粉末回折 Ptychography シェラー方程式
小角X線散乱(SAXS)
構造決定
超高速X線
広角X線散乱(WAXS)
参考文献
^ 「共鳴X線散乱|シェン研究所」。arpes.stanford.edu 。
^ ケプラーJ(1611)。Strena seu de NiveSexangula。フランクフルト:G。タンパック。ISBN
3-321-00021-0。
^ ステノN(1669)。De solido intra solidum naturaliter contento dissertationisprodromus。Florentiae。
^ ヘッセルJFC(1831)。KristallometrieまたはKristallonomieundKristallographie。ライプツィヒ。
^ ブラヴェA(1850)。「Mémoiresurlessystèmesforméspardespointsdistribuésregulièrementsurunplanou dansl’espace」。Journaldel’ÉcolePolytechnique。19:1。
^ Shafranovskii II&Belov NV(1962)ポール・イーワルド(編)。「ESフェドロフ」(PDF)。X線回折の50年。スプリンガー:351 ISBN 90-277-9029-9。
^ シェーンフリースA(1891)。Kristallsysteme undKristallstruktur。ライプツィヒ。
^ Barlow W(1883)。「結晶の内部対称性のありそうな性質」。ネイチャー。29(738):186 Bibcode:1883Natur..29..186B。土井:10.1038 / 029186a0。
Barlow、William(1883)も参照してください 。「結晶の内部対称性のありそうな性質」。ネイチャー。29(739):205 Bibcode:1883Natur..29..205B。土井:10.1038 / 029205a0。 Sohncke、L。(1884)「結晶の内部対称性のありそうな性質」。ネイチャー。29(747):383 Bibcode:1884Natur..29..383S。土井:10.1038 / 029383a0。S2CID 4072817。 バーロウ、WM。(1884)。「結晶の内部対称性のありそうな性質」。ネイチャー。29(748):404 Bibcode:1884Natur..29..404B。土井:10.1038 / 029404b0。S2CID 4016086。
^ アインシュタインA(1905)。「ÜbereinendieErzeugungund Verwandlung des Lichtes betreffenden heuristischenGesichtspunkt」 [光の創造と変換のヒューリスティックモデル]。Annalen der Physik(ドイツ語)。17(6):132 Bibcode:1905AnP … 322..132E。土井:10.1002 /andp.19053220607。
。英語の翻訳は、から入手することができウィキソース。
^ 比較: アインシュタインA(1909)。「ÜberdieEntwicklungunsererAnschauungenüberdasWesenunddie Konstitution derStrahlung」[放射線の組成と本質に関する私たちの見解の発展]。Physikalische Zeitschrift(ドイツ語)。10:817。。英語の翻訳は、から入手することができウィキソース。
^ Pais A(1982)。微妙なのは主です:アルバートアインシュタインの科学と生活。オックスフォード大学出版局。ISBN
0-19-853907-X。
^ コンプトンA(1923)。「軽元素によるX線散乱の量子論」(PDF)。物理学 改訂。21(5):483 Bibcode:1923PhRv … 21..483C。土井:10.1103 /PhysRev.21.483。
^ ブラッグWH(1907)。「レントゲン線の性質」。オーストラリア王立科学協会の取引。31:94。
^ ブラッグWH(1908)。「γ線とX線の性質」。ネイチャー。77(1995):270 Bibcode:1908Natur..77..270B。土井:10.1038 / 077270a0。S2CID 4020075。
Bragg、WH(1908)も参照してください 。「γ線とX線の性質」。ネイチャー。78(2021):271 Bibcode:1908Natur..78..271B。土井:10.1038 / 078271a0。S2CID 4039315。 ブラッグ、WH(1908)。「γ線とX線の性質」。ネイチャー。78(2022):293 Bibcode:1908Natur..78..293B。土井:10.1038 / 078293d0。S2CID 3993814。 ブラッグ、WH(1908)。「X線の性質」。ネイチャー。78(2035):665 Bibcode:1908Natur..78R.665B。土井:10.1038 / 078665b0。S2CID 4024851。
^ ブラッグWH(1910)。「γ線とX線の粒子説の結果、およびβ線の範囲」。フィル。マグ。20(117):385 DOI:10.1080 / 14786441008636917。
^ ブラッグWH(1912)。「X線によるイオン化の直接的または間接的な性質について」。フィル。マグ。23(136):647 DOI:10.1080 / 14786440408637253。
^ フリードリヒW; ニッピングP; フォンラウエM(1912年)。「Interferenz-ErscheinungenbeiRöntgenstrahlen」。Sitzungsberichte derMathematisch-PhysikalischenClassederKöniglich-BayerischenAkademiederWissenschaftenzuMünchen。1912年:303。
^ フォンラウエM(1914)。「X線干渉の検出について」(PDF)。ノーベル講義、物理学。1901〜1921 。
^ ダナES; フォードWE(1932年)。鉱物学の教科書(第4版)。ニューヨーク:ジョン・ワイリー&サンズ。NS。28。
^ アンドレ・ギニエ(1952)X線結晶学技術。ロンドン:Hilger and WattsLTD。NS。271。
^ ブラッグWL(1912)。「X線の鏡面反射」。ネイチャー。90(2250):410 Bibcode:1912Natur..90..410B。土井:10.1038 / 090410b0。S2CID 3952319。
^ ブラッグWL(1913)。「結晶による短い電磁波の回折」。ケンブリッジ哲学協会の議事録。17:43。
^ ブラッグ(1914)。「DieReflexionderRöntgenstrahlen」。JahrbuchderRadioaktivitätundElektronik。11:350。
^ ブラッグ(1913)。「X線の回折によって示されるいくつかの結晶の構造」。手順 R.Soc。Lond。A89(610):248–277。Bibcode:1913RSPSA..89..248B。土井:10.1098 /rspa.1913.0083。JSTOR 93488。
^ ブラッグWL; ジェームズRW; ボサンケットCH(1921)。「岩塩によるX線の反射の強さ」。フィル。マグ。41(243):309 DOI:10.1080 / 14786442108636225。
^ ブラッグWL; ジェームズRW; ボサンケットCH(1921)。「岩塩によるX線の反射の強さ。パートII」。フィル。マグ。42(247):1。DOI:10.1080 / 14786442108633730。
^ ブラッグWL; ジェームズRW; ボサンケットCH(1922)。「ナトリウムおよび塩素原子の原子核の周りの電子の分布」。フィル。マグ。44(261):433 DOI:10.1080 / 14786440908565188。
^ ブラッグWH。ブラッグWL(1913)。「ダイヤモンドの構造」。ネイチャー。91(2283):557 Bibcode:1913Natur..91..557B。土井:10.1038 / 091557a0。S2CID 3987932。
^ ブラッグWH; ブラッグWL(1913)。「ダイヤモンドの構造」。手順 R.Soc。Lond。A89(610):277 Bibcode:1913RSPSA..89..277B。土井:10.1098 /rspa.1913.0084。
^ ブラッグWL(1914)。「銅の結晶構造」。フィル。マグ。28(165):355 DOI:10.1080 / 14786440908635219。
^ ブラッグWL(1914)。「X線分光計による結晶の分析」。手順 R.Soc。Lond。A89(613):468 Bibcode:1914RSPSA..89..468B。土井:10.1098 /rspa.1914.0015。
^ ブラッグWH(1915)。「結晶のスピネル族の構造」。フィル。マグ。30(176):305 DOI:10.1080 / 14786440808635400。
^ 西川S(1915)。「スピネル族のいくつかの結晶の構造」。手順 東京数学。物理学 Soc。8:199。
^ ベガードL(1916)。「結晶解析の結果」。フィル。マグ。32(187):65 DOI:10.1080 / 14786441608635544。
^ アミノフG(1919)。「パイロクロイトの結晶構造」。ストックホルムGeol。フォーレン。Förh。41:407 DOI:10.1080 / 11035891909447000。
^ アミノフG(1921)。「ÜberdieStrukturdesMagnesiumhydroxids」。Z.Kristallogr。56:505。
^ ブラッグWL(1920)。「酸化亜鉛の結晶構造」。フィル。マグ。39(234):647 DOI:10.1080 / 14786440608636079。
^ bije P ; シェラーP(1916年)。””Interferenz an regellosorientiertenTeilchenimRöntgenlichtI””。PhysikalischeZeitschrift。17:277。
^ フリードリッヒW(1913)。「EineneueInterferenzerscheinungbeiRöntgenstrahlen」。PhysikalischeZeitschrift。14:317。
^ ハルAW(1917年)。「X線結晶分析の新しい方法」。物理学 改訂。10(6):661 Bibcode:1917PhRv … 10..661H。土井:10.1103 /PhysRev.10.661。
^ ベルナルJD(1924)。「グラファイトの構造」。手順 R.Soc。Lond。A106(740):749–773。JSTOR 94336。
^ ハッセルO; マックH(1924)。「ÜberdieKristallstrukturdesGraphits」。ZeitschriftfürPhysik。25(1):317 Bibcode:1924ZPhy … 25..317H。土井:10.1007 / BF01327534。S2CID 121157442。
^ ハルAW(1917年)。「鉄の結晶構造」。物理学 改訂。9(1):84 Bibcode:1917PhRv …. 9 … 83。。土井:10.1103 /PhysRev.9.83。
^ ハルAW(1917年7月)。「マグネシウムの結晶構造」。アメリカ合衆国科学アカデミー紀要。3(7):470–3。Bibcode:1917PNAS …. 3..470H。土井:10.1073 /pnas.3.7.470。PMC 1091290。PMID 16576242。
^ 「原子パターンに」。ウェルカムコレクション。2013年9月7日にオリジナルからアーカイブされました。取得した17年10月2013。
^ Wyckoff RWG; Posnjak E(1921)「塩化白金酸アンモニウムの結晶構造」。混雑する。化学。Soc。43(11):2292. DOI:10.1021 / ja01444a002。
^ ブラッグWH(1921)。「有機結晶の構造」。手順 R.Soc。Lond。34(1):33 Bibcode:1921PPSL … 34 … 33B。土井:10.1088 / 1478-7814 / 34/1/306。
^ ロンズデールK(1928)。「ベンゼン環の構造」。ネイチャー。122(3082):810 Bibcode:1928Natur.122..810L。土井:10.1038 / 122810c0。S2CID 4105837。
^ ポーリングL(1960)。化学結合の性質(第3版)。ニューヨーク州イサカ:コーネル大学出版局。ISBN
0-8014-0333-2。
^ ブラッグWH(1922)。「アントラセンの結晶構造」。手順 R.Soc。Lond。35(1):167 Bibcode:1922PPSL … 35..167B。土井:10.1088 / 1478-7814 / 35/1/320。
^ パウエルHM; Ewens RVG(1939)「鉄エネアカルボニルの結晶構造」。J.Chem。Soc。:286 DOI:10.1039 / jr9390000286。
^ バートランドJA; コットン; ドラーゼ(1963)。「メタル・メタルボンド、CsReCl多核錯体アニオン4」。混雑する。化学。Soc。85(9):1349 DOI:10.1021 / ja00892a029。
^ ロビンソンWT; ファーガソンJE; ペンフォールドBR(1963)。「CsReClにおけるアニオンの構成4」。ロンドンの化学協会の議事録:116。
^ コットンFA、カーティスNF、ハリスCB、ジョンソンBF、リパードSJ、マグーJT、他 (1964年9月)。「レニウム(III)の単核および多核化学:その顕著な同種親和性」。科学。145(3638):1305–7。Bibcode:1964Sci … 145.1305C。土井:10.1126 /science.145.3638.1305。PMID 17802015。S2CID 29700317。
^ コットンFA ; ハリス(1965)。「オクタクロロジレネート二カリウム(III)二水和物の結晶および分子構造」。無機化学。4(3):330 DOI:10.1021 / ic50025a015。
^ コットンFA(1965)。「[再における金属-金属結合2 X 8 ] 2-イオンおよび他の金属原子クラスター」。無機化学。4(3):334 DOI:10.1021 / ic50025a016。
^ Eberhardt WH; クロフォードWジュニア; リップスコムWN(1954)。「水素化ホウ素の原子価構造」。J.Chem。物理学。22(6):989 Bibcode:1954JChPh..22..989E。土井:10.1063 /1.1740320。
^ Martin TW、Derewenda ZS(1999年5月)。「名前はボンド–Hボンド」。自然構造生物学。6(5):403–6。土井:10.1038 / 8195。PMID 10331860。S2CID 27195273。
^ Dunitz JD; Orgel LE; リッチA(1956)。「フェロセンの結晶構造」。ActaCrystallographica。9(4):373 DOI:10.1107 / S0365110X56001091。
^ Seiler P; Dunitz JD(1979)。「フェロセンの無秩序な結晶構造の新しい解釈」。Acta CrystallographicaB。35(5):1068 DOI:10.1107 / S0567740879005598。
^ Wunderlich JA; メラーDP(1954)。「ツァイゼ塩の結晶構造に関する注記」。ActaCrystallographica。7:130 DOI:10.1107 / S0365110X5400028X。
^ ジャービスJAJ; Kilbourn BT; オーストンPG(1970)。「ツァイゼ塩、KPtClの結晶と分子構造の再決意3 .C 2 H 4・H 2 O. A補正」。Acta CrystallographicaB。26(6):876 DOI:10.1107 / S056774087000328X。
^ ジャービスJAJ; Kilbourn BT; オーストンPG(1971)。「ツァイゼ塩、KPtClの結晶と分子構造の再決意3 .C 2 H 4・H 2 O」。Acta CrystallographicaB。27(2):366 DOI:10.1107 / S0567740871002231。
^ RAが大好きです。Koetzle TF; ウィリアムズGJB; アンドリュースLC; バウR(1975)。””ツァイゼ塩の構造の中性子回折研究、KPtCl 3(C 2 H 4)・H 2 O””。無機化学。14(11):2653. DOI:10.1021 / ic50153a012。
^ Hävecker、Michael; ヴラベッツ、サビーネ; Kröhnert、Jutta; Csepei、Lenard-Istvan; ナウマン・ダルノンコート、ラウル; Kolen’Ko、Yury V。; Girgsdies、フランク; Schlögl、Robert; Trunschke、Annette(2012)。「プロパンのアクリル酸への選択的酸化における操作中の相純粋なM1MoVTeNb酸化物の表面化学」。Journal ofCatalysis。285:48–60。土井:10.1016 /j.jcat.2011.09.012。hdl:11858 / 00-001M-0000-0013-FB1F-C。
^ MoおよびVベースの混合酸化物触媒でのプロパン酸化の速度論的研究。2011年。
^ Naumann d’Alnoncourt、Raoul; Csepei、Lénárd-István; ヘベッカー、マイケル; Girgsdies、フランク; シュスター、マンフレッドE。; Schlögl、Robert; Trunschke、Annette(2014)。「相純粋なMoVTeNbM1酸化物触媒上でのプロパン酸化における反応ネットワーク」。Journal ofCatalysis。311:369–385。土井:10.1016 /j.jcat.2013.12.008。hdl:11858 / 00-001M-0000-0014-F436-1。
^ ブラウン、ドウェイン(2012年10月30日)。「NASAローバーの最初の土壌研究は火星の鉱物の指紋を助ける」。NASA 。
^ ウェストグレンA; PhragménG(1925)。「Cu-Zn、Ag-ZnおよびAu-Zn合金のX線分析」。フィル。マグ。50:311 DOI:10.1080 / 14786442508634742。
^ ブラッドリーAJ; Thewlis J(1926)。「γ-真ちゅうの構造」。手順 R.Soc。Lond。112(762):678 Bibcode:1926RSPSA.112..678B。土井:10.1098 /rspa.1926.0134。
^ ヒュームロザリーW(1926)。「金属間化合物の性質、特性および形成条件に関する研究(特にスズの特定の化合物に関連して)」。金属研究所のジャーナル。35:295。
^ ブラッドリーAJ; グレゴリーCH(1927)。「特定の三元合金の構造」。ネイチャー。120(3027):678 Bibcode:1927Natur.120..678。。土井:10.1038 / 120678a0。
^ Westgren A(1932)。「ZurChemiederLegierungen」。アンゲヴァンテケミー。45(2):33 DOI:10.1002 / ange.19320450202。
^ ベルナルJD(1935)。「金属の電子理論」。化学の進歩に関する年次報告書。32:181 DOI:10.1039 / AR9353200181。
^ ポーリングL(1923)。「マグネシウムスタニドの結晶構造」。混雑する。化学。Soc。45(12):2777. DOI:10.1021 / ja01665a001。
^ ポーリングL(1929)。「錯イオン結晶の構造を決定する原理」。混雑する。化学。Soc。51(4):1010 DOI:10.1021 / ja01379a006。
^ ディキンソンRG; レイモンドAL(1923)。「ヘキサメチレンテトラミンの結晶構造」(PDF)。混雑する。化学。Soc。45:22. DOI:10.1021 / ja01654a003。
^ ミュラーA(1923)。「脂肪酸のX線調査」。Journal of the ChemicalSociety。123:2043 DOI:10.1039 / ct9232302043。
^ Saville WB; シアラーG(1925)。「飽和脂肪族ケトンのX線調査」。Journal of the ChemicalSociety。127:591 DOI:10.1039 / ct9252700591。
^ ブラッグWH(1925)。「X線による薄膜の調査」。ネイチャー。115(2886):266 Bibcode:1925Natur.115..266B。土井:10.1038 / 115266a0。
^ Broglie M ; Trillat JJ(1925)。「Surl’interprétationphysiquedesspectersXd’acidesgras」。Comptesrendushebdomadairesdesséancesdel’Académiedessciences。180:1485。
^ Trillat JJ(1926)。「RayonsXetComposeésorganiquesàlongechaine。Recherchesspectrographiquesは、ルアー構造とルアーオリエンテーションを訴えます」。Annales dePhysique。6:5。DOI:10.1051 / anphys / 192610060005。
^ Caspari WA(1928)。「脂肪族ジカルボン酸の結晶学」。Journal of the ChemicalSociety。?:3235 DOI:10.1039 / jr9280003235。
^ ミュラーA(1928)。「長鎖化合物(n。炭化水素)のX線調査」。手順 R.Soc。ロンド。120(785):437 Bibcode:1928RSPSA.120..437M。土井:10.1098 /rspa.1928.0158。
^ パイパーSH(1929)。「脂肪酸の長い間隔から得られる情報のいくつかの例」。ファラデー協会の取引。25:348 DOI:10.1039 / tf9292500348。
^ ミュラーA(1929)。「炭化水素鎖のジグザグ構造と奇数および偶数の鎖化合物の特性の変化との関係」。手順 R.Soc。Lond。124(794):317 Bibcode:1929RSPSA.124..317M。土井:10.1098 /rspa.1929.0117。
^ ロバートソンJM(1936年)。「フタロシアニンのX線研究、パートII」。化学会誌:1195 DOI:10.1039 / jr9360001195。
^ クロウフットホジキンD(1935)。「インスリンのX線単結晶写真」。ネイチャー。135(3415):591 Bibcode:1935Natur.135..591C。土井:10.1038 / 135591a0。S2CID 4121225。
^ Kendrew JC、Bodo G、Dintzis HM、Parrish RG、Wyckoff H、Phillips DC(1958年3月)。「X線分析によって得られたミオグロビン分子の3次元モデル」。ネイチャー。181(4610):662–6。Bibcode:1958Natur.181..662K。土井:10.1038 / 181662a0。PMID 13517261。S2CID 4162786。
^ 「1962年のノーベル化学賞」。www.nobelprize.org 。
^ 「実験的な方法で整理されたPDBのエントリの表」。
^ 「PDB統計」。RCSBタンパク質データバンク。
^ Scapin G(2006)。「構造生物学と創薬」。現在の薬理学的デザイン。12(17):2087–97。土井:10.2174 / 138161206777585201。PMID 16796557。
^ Lundstrom K。「膜タンパク質の構造ゲノミクス」。細胞および分子生命科学。63(22):2597–607。土井:10.1007 / s00018-006-6252-y。PMID 17013556。S2CID 13432321。
^ Lundstrom K。「膜タンパク質の構造ゲノミクス:ミニレビュー」。コンビナトリアルケミストリーとハイスループットスクリーニング。7(5):431–9。土井:10.2174 / 1386207043328634。PMID 15320710。
^ Chinte U、Shah B、Chen YS、Pinkerton AA、Schall CA、Hanson BL。「極低温(<20 K)ヘリウム冷却は、タンパク質結晶への放射線損傷を軽減します」。ActaCrystallographica。セクションD、生物学的結晶学。63(Pt 4):486–92。土井:10.1107 / s0907444907005264。PMID 17372353。
^ Claydon、J。; グリーブス、N。およびウォーレン、S。(2012)。有機化学(PDF)(第2版)。オックスフォード大学出版局。NS。45. ISBN 978-0199270293。
^ Baskaran K、Duarte JM、Biyani N、Bliven S、Capitani G。「タンパク質間相互作用のPDB全体の進化ベースの評価」。BMC構造生物学。14(1):22 DOI:10.1186 / s12900-014-0022-0。PMC 4274722。PMID 25326082。
^ Levy ED。「PiQSi:タンパク質の四次構造の調査」。構造。15(11):1364–7。土井:10.1016 /j.str.2007.09.019。PMID 17997962。
^ Suryanarayana、C。; ノートン、M。グラント(2013-06-29)。X線回折:実用的なアプローチ。シュプリンガーサイエンス&ビジネスメディア。ISBN
9781489901484。
^ グレイリンガー、オールデンB(1935)。「結晶方位を決定するための後方反射ラウエ法」。ZeitschriftfürKristallographie-結晶学材料。91(1–6)。土井:10.1524 /zkri.1935.91.1.424。S2CID 101434745。
^ コンパクトディスクまたはDVDにレーザーポインターを当てると、同様の回折パターンが観察される場合がCDトラックの周期的な間隔は、結晶内の原子の周期的な配置に対応します。
^ 「形態学XRD分析| IMRテストLABS」。www.imrtest.com 。
^ ジョーンズN。「結晶学:原子の秘密」。ネイチャー。505(7485):602–3。Bibcode:2014Natur.505..602J。土井:10.1038 / 505602a。PMID 24476871。
^ Miao、Jianwei; Charalambous、Pambos; キルツ、ヤノス; Sayre、David(1999)。「X線結晶学の方法論を拡張して、マイクロメートルサイズの非結晶試料のイメージングを可能にします」。ネイチャー。400(6742):342 Bibcode:1999Natur.400..342M。土井:10.1038 / 22498。S2CID 4327928。
^ Harp JM、Timm DE、Bunick GJ(1998年7月)。「高分子結晶アニーリング:低温結晶学に関連するモザイク性の増加の克服」。ActaCrystallographica。セクションD、生物学的結晶学。54(Pt 4):622–8。土井:10.1107 / S0907444997019008。PMID 9761858。
^ Harp JM、Hanson BL、Timm DE、Bunick GJ(1999年7月)。「高分子結晶アニーリング:技術と変数の評価」。ActaCrystallographica。セクションD、生物学的結晶学。55(Pt 7):1329–34。土井:10.1107 / S0907444999005442。PMID 10393299。
^ Hanson BL、Harp JM、Bunick GJ(2003)。「平均律クラヴィーア曲集:高分子結晶のアニーリング」。高分子の結晶学、パートC。酵素学の方法。368。pp。217–35。土井:10.1016 / S0076-6879(03)68012-2。ISBN
978-0-12-182271-2。PMID 14674276。
^ Geerlof A、Brown J、Coutard B、Egloff MP、Enguita FJ、FoggMJなど。。「構造プロテオミクスにおけるタンパク質特性の影響」。ActaCrystallographica。セクションD、生物学的結晶学。62(Pt 10):1125–36。土井:10.1107 / S0907444906030307。PMC 7161605。PMID 17001090。
^ Chernov AA。「タンパク質の結晶とその成長」。構造生物学ジャーナル。142(1):3–21。土井:10.1016 / S1047-8477(03)00034-0。PMID 12718915。
^ Terese Bergfors(2016)。「タンパク質結晶化チュートリアル」。
^ チャイエン、ナオミ。「油の下での結晶化の限界」。
^ Rupp B、Wang J。「タンパク質結晶化の予測モデル」。メソッド。34(3):390–407。土井:10.1016 /j.ymeth.2004.03.031。PMID 15325656。
^ Chayen NE。「タンパク質結晶化における核形成と成長を分離するための方法」。生物物理学と分子生物学の進歩。88(3):329–37。土井:10.1016 /j.pbiomolbio.2004.07.007。PMID 15652248。
^ ストックD、ペリシッチO、レーヴェJ。「MRC分子生物学研究所でのロボットナノリットルタンパク質の結晶化」。生物物理学と分子生物学の進歩。88(3):311–27。土井:10.1016 /j.pbiomolbio.2004.07.009。PMID 15652247。
^ Jeruzalmi D(2006)。「高分子結晶の最初の分析:生化学とX線回折」。高分子結晶学プロトコル、第2巻。分子生物学の方法。364。pp。43–62。土井:10.1385 / 1-59745-266-1:43。ISBN
1-59745-266-1。PMID 17172760。
^ Helliwell JR。「タンパク質結晶の完成度とその応用」。ActaCrystallographica。セクションD、生物学的結晶学。61(Pt 6):793–8。土井:10.1107 / S0907444905001368。PMID 15930642。
^ Vandenberg JM、Temkin H、Hamm RA、DiGiuseppe MA(1982)。「InGaAsP / InP層上の合金化された金のメタライゼーション接点の構造研究」。Journal of AppliedPhysics。53(11):7385–7389。Bibcode:1982JAP …. 53.7385V。土井:10.1063 /1.330364。
^ Vandenberg JM、Temkin H(1984)。「InGaAsP / InP層との金/バリア金属相互作用のその場X線研究」。Journal of AppliedPhysics。55(10):3676–3681。Bibcode:1984JAP …. 55.3676V。土井:10.1063 /1.332918。
^ ガーマン、EF; シュナイダー、TR(1997)。「高分子低温結晶学」。応用結晶学ジャーナル。30(3):211 DOI:10.1107 / S0021889897002677。
^ Schlichting I、Miao J。「X線自由電子レーザーによる構造生物学の新たな機会」。構造生物学における現在の意見。22(5):613–26。土井:10.1016 /j.sbi.2012.07.015。PMC 3495068。PMID 22922042。
^ Neutze R、Wouts R、van der Spoel D、Weckert E、Hajdu J。「フェムト秒X線パルスによる生体分子イメージングの可能性」。ネイチャー。406(6797):752–7。Bibcode:2000Natur.406..752N。土井:10.1038 / 35021099。PMID 10963603。S2CID 4300920。
^ Liu W、Wacker D、Gati C、Han GW、James D、Wang D、他 。「Gタンパク質共役型受容体のシリアルフェムト秒結晶学」。科学。342(6165):1521–4。Bibcode:2013Sci … 342.1521L。土井:10.1126 /science.1244142。PMC 3902108。PMID 24357322。
^ Ravelli RB、Garman EF。「高分子低温結晶学における放射線損傷」。構造生物学における現在の意見。16(5):624–9。土井:10.1016 /j.sbi.2006.08.001。PMID 16938450。
^ パウエルHR(1999年10月)。「MOSFLMのロスマンフーリエ自動索引付けアルゴリズム」。ActaCrystallographica。セクションD、生物学的結晶学。55(Pt 10):1690–5。土井:10.1107 / S0907444999009506。PMID 10531518。
^ ハウプトマンH(1997年10月)。「タンパク質結晶学のための位相調整法」。構造生物学における現在の意見。7(5):672–80。土井:10.1016 / S0959-440X(97)80077-2。PMID 9345626。
^ UsónI、シェルドリックGM(1999年10月)。「タンパク質結晶学のための直接法の進歩」。構造生物学における現在の意見。9(5):643–8。土井:10.1016 / S0959-440X(99)00020-2。PMID 10508770。
^ テイラーG。「位相問題」。ActaCrystallographica。セクションD、生物学的結晶学。59(Pt 11):1881–90。土井:10.1107 / S0907444903017815。PMID 14573942。
^ Ealick SE。「多波長異常分散結晶学の進歩」。化学生物学における現在の意見。4(5):495–9。土井:10.1016 / S1367-5931(00)00122-8。PMID 11006535。
^ PDBファイル2NRL、残基17〜32から。
^ http://proteopedia.org/wiki/index.php/Garman_lab:_Interconversion_of_lysosine_enzyme_specificities、
^ パーキンG(1993)。「遷移金属錯体におけるボンドストレッチ異性:結晶学的データの再評価」。化学。改訂。93(3):887–911。土井:10.1021 / cr00019a003。
^ リートフェルト、HM(1969-06-02)。「核および磁気構造のプロファイル改良法」。応用結晶学ジャーナル。2(2):65–71。土井:10.1107 / S0021889869006558。
^ リートベルト法。ヤング、RA(ロバート・アラン)、1921年-。:Crystallograhyの国際連合。1993年。ISBN
0198555776。OCLC 26299196。
^ 「IUCr」。www.iucr.org 。
^ 「Fullprof」。www.ill.eu 。
^ Petříček、Václav; デュシェック、ミハル; パラティヌス、ルカシュ(2014-01-01)。「結晶計算システムJANA2006:一般的な機能」。ZeitschriftfürKristallographie-結晶学材料。229(5)。土井:10.1515 / zkri-2014-1737。ISSN 2196から7105まで。S2CID 101692863。
^ Lutterotti、Luca。「薄膜回折におけるサイズ-ひずみ-応力-テクスチャの決定を組み合わせたトータルパターンフィッティング」。物理学研究セクションBの核機器と方法:材料と原子とのビーム相互作用。268(3–4):334–340。Bibcode:2010NIMPB.268..334L。土井:10.1016 /j.nimb.2009.09.053。ISSN 0168-583X。
^ Lutterotti、L。; Bortolotti、M。; イスキア、G。; Lonardelli、I。; ウェンク、H.-R。(2007)、「回折画像からのRietveldテクスチャ分析」、第10回欧州粉末回折会議、OLDENBOURG WISSENSCHAFTSVERLAG、doi:10.1524 / 9783486992540-020、ISBN 9783486992540 ^ Lutterotti、L。; Matthies、S。; ウェンク、H.-R。; シュルツ、AS; リチャードソン、JW(1997-01-15)。「飛行時間型中性子回折スペクトルからの変形した石灰岩のテクスチャと構造を組み合わせた分析」。Journal of AppliedPhysics。81(2):594–600。Bibcode:1997JAP …. 81..594L。土井:10.1063 /1.364220。ISSN 0021から8979まで。
^ 「RIETAN-FP-VENUSパッケージの配布ファイル」。fujioizumi.verse.jp 。
^ トビー、ブライアンH。; Von Dreele、Robert B.(2013-03-14)。「GSAS-II:最新のオープンソースの万能結晶学ソフトウェアパッケージの起源」。応用結晶学ジャーナル。46(2):544–549。土井:10.1107 / s0021889813003531。ISSN 0021から8898まで。
^ 「DIFFRAC.SUITETOPAS-XRDソフトウェア、X線回折」。Bruker.com 。
^ 「一致!-粉末回折からの相同定」。www.crystalimpact.com 。
^ カサス-カバナ、モンセ; レイノー、マリン; リカルテ、ジョキン; Horbach、Pavel; Rodríguez-Carvajal、Juan(2016-12-01)。「FAULTS:拡張された欠陥を持つ構造の改良のためのプログラム」。応用結晶学ジャーナル。49(6):2259–2269。土井:10.1107 / S1600576716014473。ISSN 1600から5767まで。
^ パターソンAL(1935)。「結晶中の原子間距離の成分を決定するための直接法」。ZeitschriftfürKristallographie。90(1-6):517 DOI:10.1524 / zkri.1935.90.1.517。S2CID 102041995。
^ 「1914年のノーベル物理学賞」。ノーベル財団。
^ 「1915年のノーベル物理学賞」。ノーベル財団。
^ 「1962年のノーベル化学賞」。Nobelprize.org 。
^ 「生理学または医学のノーベル賞1962年」。ノーベル財団。
^ 「1964年のノーベル化学賞」。Nobelprize.org 。
^ 「1972年のノーベル化学賞」。Nobelprize.org 。
^ 「1976年のノーベル化学賞」。Nobelprize.org 。
^ 「1985年のノーベル化学賞」。Nobelprize.org 。
^ 「1988年のノーベル化学賞」。Nobelprize.org 。
^ 「1997年のノーベル化学賞」。Nobelprize.org 。
^ 「化学2003年のノーベル賞」。Nobelprize.org 。
^ 「2006年のノーベル化学賞」。Nobelprize.org 。
^ 「2009年のノーベル化学賞」。Nobelprize.org 。
^ 「2012年ノーベル化学賞」。Nobelprize.org 。
^ マックス・フォン・ラウエ(1937)。ラウエ図。バンガロールプレス。NS。9.9。
^ フランス、AndréAuthier、InstitutdeMinéralogieetdePhysique desMilieuxCondensés、UniversitéP。et M. Curie、パリ(2013)。X線結晶学の初期(初版)。オックスフォード:オックスフォード大学出版局。pp。1–8。ISBN
9780199659845。
^ Thangadurai S、Abraham JT、Srivastava AK、Moorthy MN、Shukla SK、Anjaneyulu Y。「特定のベータラクタム、テトラサイクリンおよびマクロライド抗生物質のX線粉末回折パターン」。分析科学。21(7):833–8。土井:10.2116 /analsci.21.833。PMID 16038505。
^ レンドルDF。「法医学に適用される化学の進歩」。化学協会レビュー。34(12):1021–30。土井:10.1039 / b415890n。PMID 16284668。
^ 「100MeVの金イオン照射による酸化グラフェンとグラファイトの構造的、機能的、磁気的秩序の変化」。真空。182:109700。2020-12-01。doi:10.1016 / j.vacuum.2020.109700
^ Zhang、JY、Boyd、IW、O’sullivan、BJ、Hurley、PK、Kelly、PVおよびSenateur、JP、2002。光学、XRDおよびFTIR分光法によって研究されたナノ結晶TiO2フィルム。Journal of Non-Crystalline Solids、303(1)、pp.134-138。https://doi.org/10.1016/S0022-3093(02)00973-0
^ Chavan、SM、MK Babrekar、SS More、およびKMJadhav。「ナノ結晶Ni–Znフェライト薄膜の構造的および光学的特性。」Journal of Alloys and Compounds 507、no。1(2010):21-25。https://doi.org/10.1016/j.jallcom.2010.07.171
^ Badri、Muhammad Ashraf Saiful、Muhamad Mat Salleh、Noor Far’ain Md Noor、Mohd Yusri Abd Rahman、およびAkrajas AliUmar。「グラフェン薄膜調製のための水性処理グラファイト剥離からの数層グラフェンのグリーン合成。」Materials Chemistry and Physics 193(2017):212-219。https://doi.org/10.1016/j.matchemphys.2017.02.029
^ SvarcováS、KocíE、Bezdicka P、Hradil D、HradilováJ。「文化遺産および法医学の分野での応用のための実験室粉末X線微小回折の評価」。分析および生物分析化学。398(2):1061–76。土井:10.1007 / s00216-010-3980-5。PMID 20640895。S2CID 11891108。
^ Hiller JC、Thompson TJ、Evison MP、Chamberlain AT、Wess TJ。「実験的加熱中の骨ミネラル変化:X線散乱調査」。生体材料。24(28):5091–7。土井:10.1016 / s0142-9612(03)00427-7。PMID 14568425。
^ コートランド、レイチェル(2017年3月17日)。「X線は集積回路の3D内部をマッピングします」。IEEEスペクトラム:テクノロジー、エンジニアリング、およびサイエンスニュース。
参考文献
結晶学のための国際的な表
テオ・ハーン編 (2002)。結晶学のための国際的な表。ボリュームA、空間群対称性(第5版)。Dordrecht:Kluwer Academic Publishers、国際結晶学連合。ISBN 0-7923-6590-9。
マイケルG.ロスマン; エディ・アーノルド編 (2001)。結晶学のための国際的な表。ボリュームF、生体分子の結晶学。Dordrecht:国際結晶学連合のKluwer AcademicPublishers。ISBN 0-7923-6857-6。
テオ・ハーン編 (1996)。結晶学のための国際的な表。ボリュームAの簡単な教育版、空間群対称性(第4版)。Dordrecht:国際結晶学連合のKluwer AcademicPublishers。ISBN 0-7923-4252-6。
記事のバインドされたコレクション
チャールズW.カーター; ロバート・M・スウィート編 (1997)。高分子結晶学、パートA(酵素学の方法、v。276)。サンディエゴ:アカデミックプレス。ISBN 0-12-182177-3。
チャールズW.カータージュニア; ロバート・M・スウィート編 (1997)。高分子結晶学、パートB(酵素学の方法、v。277)。サンディエゴ:アカデミックプレス。ISBN 0-12-182178-1。
A. Ducruix; R.Giegé編 (1999)。核酸とタンパク質の結晶化:実用的なアプローチ(第2版)。オックスフォード:オックスフォード大学出版局。ISBN 0-19-963678-8。
教科書
Birkholz M、FewsterPFおよびGenzelC(2005)による寄稿。「第1章:Principles_of_X-ray_Diffraction」。X線散乱による薄膜分析。ヴァインハイム:Wiley-VCH。ISBN 978-3-527-31052-4。
ブローD(2002)。生物学者のための結晶学の概要。オックスフォード:オックスフォード大学出版局。ISBN 0-19-851051-9。
バーンズG .; Glazer AM(1990)。科学者とエンジニアのための空間群(第2版)。ボストン:アカデミックプレス社ISBN 0-12-145761-3。
クレッグW(1998)。結晶構造決定(オックスフォード化学入門書)。オックスフォード:オックスフォード大学出版局。ISBN 0-19-855901-1。
カリティーBD(1978)。X線回折の要素(第2版)。マサチューセッツ州レディング:Addison-Wesley Publishing Company ISBN 0-534-55396-6。
Drenth J(1999)。タンパク質X線結晶学の原理。ニューヨーク:Springer-Verlag。ISBN 0-387-98587-5。
ジャコヴァッツォC(1992)。結晶学の基礎。オックスフォード:オックスフォード大学出版局。ISBN 0-19-855578-4。
Glusker JP; ルイスM; ロッシM(1994)。化学者および生物学者のための結晶構造分析。ニューヨーク:VCHパブリッシャー。ISBN 0-471-18543-4。
マッサW(2004)。結晶構造の決定。ベルリン:スプリンガー。ISBN 3-540-20644-2。
マクファーソンA(1999)。生体高分子の結晶化。ニューヨーク州コールドスプリングハーバー:コールドスプリングハーバーラボラトリープレス。ISBN 0-87969-617-6。
マクファーソンA(2003)。高分子結晶学入門。ジョンワイリー&サンズ。ISBN 0-471-25122-4。
マクリーDE(1993)。実用的なタンパク質結晶学。サンディエゴ:アカデミックプレス。ISBN 0-12-486050-8。
オキーフM; ハイドBG(1996)。結晶構造; I.パターンと対称性。ワシントンDC:アメリカ鉱物学会、モノグラフシリーズ。ISBN 0-939950-40-5。
ロードスG(2000)。結晶学はクリスタルクリアになりました。サンディエゴ:アカデミックプレス。ISBN 0-12-587072-8。、選択した章のPDFコピー
ラップB(2009)。生体分子結晶学:原理、実践および構造生物学への応用。ニューヨーク:ガーランドサイエンス。ISBN 978-0-8153-4081-2。
ウォーレンBE(1969)。X線回折。ニューヨーク。ISBN 0-486-66317-5。
Zachariasen WH(1945)。結晶におけるX線回折の理論。ニューヨーク:ドーバー出版。LCCN 67026967。
応用計算データ分析
ヤング、RA、編 (1993)。リートベルト法。オックスフォード:オックスフォード大学出版局および国際結晶学連合。ISBN 0-19-855577-6。
歴史的
Bijvoet JM ; ハンバーガーWG; ヘッグG; eds。(1969)。結晶によるX線の回折に関する初期の論文。私。ユトレヒト:A。OosthoekのUitgeversmaatschappijNVによって国際結晶学連合のために公開されました
Bijvoet JM; ハンバーガーWG; ヘッグG編 (1972)。結晶によるX線の回折に関する初期の論文。II。ユトレヒト:A。OosthoekのUitgeversmaatschappijNVによって国際結晶学連合のために公開されました
ブラッグWL; フィリップスDC&リプソンH(1992)。X線分析の開発。ニューヨーク:ドーバー。ISBN 0-486-67316-2。
エヴァルト、PP ; そして多くの結晶学者、編。(1962年)。X線回折の50年。ユトレヒト:A。OosthoekのUitgeversmaatschappij NV doi:10.1007 / 978-1-4615-9961-6によって国際結晶学連合のために公開されました。ISBN 978-1-4615-9963-0。
Ewald、PP、編集者50 Years of X-Ray Diffraction(IUCr XVIII Congress、グラスゴー、スコットランド、国際結晶学連合のためにpdf形式で転載)。
フリードリヒW(1922)。”Die GeschichtederAuffindungderRöntgenstrahlinterferenzen”。Naturwissenschaftenを死ぬ。10(16):363 Bibcode:1922NW ….. 10..363F。土井:10.1007 / BF01565289。S2CID 28141506。
ロンズデール、K(1949年)。結晶とX線。ニューヨーク:D。ヴァンノストランド。
「生命の構造」。米国保健社会福祉省。2007年。
外部リンク
ウィキブックスには、次のトピックに関する本があります:X線結晶学
チュートリアル
結晶学を学ぶ
シンプルで非技術的な紹介
結晶学コレクション、王立機関からのビデオシリーズ
イリノイ工科大学のウェブサイトにある「小分子結晶化」(PDF)
国際結晶学連合
結晶学101
2D結晶の回折パターンの特性を示すインタラクティブな構造因子チュートリアル。
フーリエ変換の絵本。結晶と回折パターンの関係を2Dで示しています。
X線結晶学と構造決定に関する講義ノート
Richard J.Matyiによるナノスケール材料分析のための最新のX線散乱法に関するオンライン講義
王立機関からのインタラクティブ結晶学タイムライン
一次データベース
結晶学オープンデータベース(COD)
Protein Data Bank(PDB)
核酸データバンク(NDB)
ケンブリッジ構造データベース(CSD)
無機結晶構造データベース(ICSD)
生体高分子結晶化データベース(BMCD)
派生データベース PDBsum Proteopedia –タンパク質やその他の分子の共同3D百科事典 RNABase PDBリガンドのHIC-Upデータベース
タンパク質データベースの構造分類
CATHタンパク質構造分類
既知の3D構造を持つ膜貫通タンパク質のリスト
膜データベース内のタンパク質の配向
構造検証
MolProbity構造検証スイート ProSA-web NQ-フリッパー(AsnおよびGln残基の好ましくない回転異性体をチェックします)
DALIサーバー(特定のタンパク質に類似したタンパク質を識別します)”